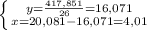
V(р-ра HNO3)=0,81 мл
Объяснение:
сантимолярный раствор - это значит, что в 1 литре раствора содержится сантимоль вещества или 0,01 моль вещества.
Значит в 0,5 литрах его будет в 2 раза меньше 0,01/2=0,005 моль.
Найдем молярную массу азотной кислоты:
Mr(HNO3)=1+14+3*16=63 г/моль
Воспользуемся формулой:
n=m/Mr, где Mr - молярная масса любого вещества
отсюда m=n*Mr
m(HNO3)=0,005*63=0,315 г
Найдем массу 30% раствора. Для этого составим пропорцию:
30% составляет 0,315 г HNO3
100% составляет - Х г
Отсюда m=Х=0,315*100/30=1,05 грамма раствора
Воспользуемся формулой:
m=p*V V=m/p
Получим: V(р-ра HNO3)=1,05/1,3=0,81 мл
m2 = m1W1/W2 = 12x0,02/0,05 = 4,8 кг - это масса 5%-ного раствора соли, которая включает в себя еще и массу воды, масса соли равна: m(соли) = m(p-pa)xW = 4,8x0,05 = 0,24 кг = 240 г.