90 г 128 г X г
СH3COOH + C2H5OH = СH3COOC2H5 + H2O
60 г 46 г 88 г
Напишем все изветное над и под уравнением.
Найдем массы интересующих веществ по уравнению:
m=M x n
m(СH3COOH) = 60гр/моль х 1 моль = 60гр
m(C2H5OH)=46гр/моль х 1 моль = 46гр
m(СH3COOC2H5)=88гр/моль х 1 моль = 88гр
Теперь найдем какого вещества взято в избытке:
Для удобства расчета за х примем массу C2H5OH и найдем, какое из веществ, вступивших в реакцию, дано в избытке, какое – в недостатке.
90 г СH3COOH - Хгр C2H5OH
60 г СH3COOH- 46 г C2H5OH
Cоставим пропорцию:
90 г /60 г = Х г / 46 г
m(C2H5OH) = 90 г х 46 г / 60 г = 69гр
Значит, C2H5OH дан в недостатке т. к. по условию его 128 г, а по расчету необходимо 69 г, поэтому расчет ведем по C2H5OH:
Составляем пропорцию и находим массу эфира теоретически:
128 г / 46 г = Х г / 88 г
m(СH3COOC2H5) = 128 г х 88 г / 46 г =245 г
Теперь найдем массу эфмра практически:
ω = m(прак) х 100% / m( теор)
m(прак) = ω х m( теор) / 100%
m (СH3COOC2H5) = 85% х 245 г / 100% = 208,25 г
1. А) N2 + 3Н2 = 2NН3 - соединения
Б) 3Mg + 2H3РО4 = Mg3(РО4)2 +3 H2↑ - замещения
В) 2Al(OH)3 = Al2O3 + 3H2O - разложения
Г) 2Cu2O = 4Cu + O2↑ - разложения
2. Na2CO3 + 2HCl = 2NaCl + H2O + CO2 - ионного обмена.
признаки: выделение воды и газа, индикатор показывает нейтральный pH (в первом растворе (Na2CO3) изначально показывалась щелочная среда, во втором (HCl) - кислая)
2 + + 2+2=2+2+ H2O + CO2
+ 2=H2O + CO2
3. 2Mg+O2=2MgO
Магний+кислород=оксид магния
MgO+2HCl=MgCl2+H2O
оксид магния+соляная кислота=хлорид магния +вода
MgCl2+2KOH=Mg(OH)2+2KCl
хлорид магния+гидроксид калия= гидроксид магния + хлорид калия
4. 2 + 6 =2 +3
--3e-> 3 2 окислитель
2-+2e-> 2 3 восстановитель
Объяснение:
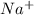

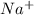
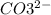

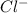
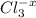


Vm=22.4
V(CO2)=22.4
8.96/22.4=x/175
x=70
ответ: 70