1) 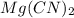 ⇒
⇒ 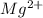 + 2
+ 2 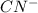
Гидролиз протекает и по катиону и по аниону, т.к соль образована слабым основанием и слабой кислотой.
Протолитическая форма:
Гидролиз по катиону:
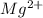 + 4
+ 4 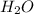 ⇔
⇔ ![[Mg(H_{2} O)_{4})]^{2+}](/tpl/images/2101/8856/6e7cd.png)
![[Mg(H_{2} O)_{4})]^{2+} + H_{2} O](/tpl/images/2101/8856/78463.png) ⇔
⇔ ![[Mg(OH)(H_{2}O)_{3}]^+ + H_{3}O^{+}](/tpl/images/2101/8856/88773.png)
![[Mg(OH)(H_{2}O)_{3}]^+ + H_{2}O](/tpl/images/2101/8856/a689f.png) ⇔
⇔ ![[Mg(OH)_{2}(H_{2}O)_{2}] + H_{3}O^{+}](/tpl/images/2101/8856/6abe3.png)
Краткое ионное уравнение:
1 ступень: 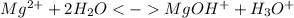
2 ступень: 
Гидролиз по аниону:
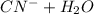 ⇔
⇔ 
Молекулярное ур-е: 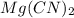 + 2
+ 2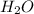 ⇔
⇔ 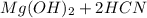 , среда слабощелочная, т.к константа диссоциации основания Mg(OH)2 > константы диссоциации кислоты HCN.
, среда слабощелочная, т.к константа диссоциации основания Mg(OH)2 > константы диссоциации кислоты HCN.
2) Rb₂SO₃ ⇒ 2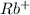 +
+ 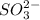
Соль образована сильным основанием и слабой кислотой, гидролиз идет по аниону.
Краткое ионное уравнение гидролиза:
Гидролиз по аниону:
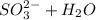 ⇔
⇔ 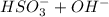 - первая ступень
- первая ступень
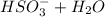 ⇔
⇔ 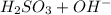 - вторая ступень
- вторая ступень
Молекулярное ур-е: 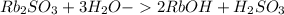
Среда щелочная, т.к в итоге выделились гидроксид ионы, pH>7. Также степень диссоциации основания > степени диссоциации кислоты, из чего можно сделать вывод, что среда - кислая.
3) 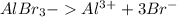
Соль образована слабым основанием и сильной кислотой, поэтому гидролиз идет по катиону.
Протолитическая форма:
![Al^{3+}+6H_2O [Al(H_2O)_6]^{3+}](/tpl/images/2101/8856/df26b.png)
![[Al(H_2O)_6]^{3+} + H_2O [Al(OH)(H_2O)_5]^{2+} + H_3O^+](/tpl/images/2101/8856/9396d.png)
![[Al(OH)(H_2O)_5]^{2+} + H_2O [Al(OH)_2(H_2O)_4]^{+} +H_3O^+](/tpl/images/2101/8856/c0d01.png)
![[Al(OH)_2(H_2O)_4]^+ + H_2O [Al(OH)_3(H_2O)_3] + H_3O^+](/tpl/images/2101/8856/62398.png)
Молекулярное ур-е: 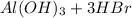
Сокращенное ионное уравнение:
1 ступень: 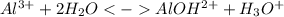
2 ступень: 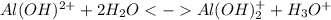
3 ступень: 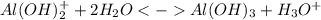
Среда кислая из-за образования ионов гидроксония. Также константа диссоциации основания < степени диссоциации кислоты, это также подтверждает, что среда кислая.
4) 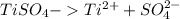
Соль образована слабым основанием и сильной кислотой, гидролиз протекает по катиону:
Протолитическая форма:
![Ti^{2+} + 4H_2O - [Ti(H_2O)4]^{2+}](/tpl/images/2101/8856/abb19.png)
![[Ti(H_2O)_4]^{2+}+H_2O [Ti(OH)(H_2O)_3]^++H_3O^+](/tpl/images/2101/8856/852e0.png)
![[Ti(OH)(H_2O)_3]^++H_2O [Ti(OH)_2(H_2O)_2] + H_3O^+](/tpl/images/2101/8856/d3bc2.png)
Молекулярное ур-е: 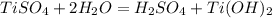
Сокращенное ионное уравнение:
1 стадия: 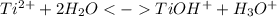
2 стадия: 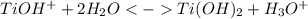
Среда кислая из-за присутствия ионов гидроксония. Также степень диссоциации основания < степени диссоциации кислоты, следовательно среда будет кислая, pH<7.
Дано:
P(смеси) = 202,6 кПа
φ(Cl₂) = 40,7% = 0,407
---------------------------------
Найти:
P(PCl₅) - ?
1) Для начала мы запишем уравнение реакций то что известно из условия задачи:
PCl₅ → PCl₃ + Cl₂
2) По уравнению реакции количество вещества образовавшихся веществ у хлора и трихлорида фосфора к моменту равновесия будут равны:
n(Cl₂) = n(PCl₃)
3) Тогда по закону Авогадро объемы хлора и трихлорида фосфора к моменту равновесия будут тоже самое равны:
V(Cl₂) = V(PCl₃)
4) Объемные доли компонентов газовой смеси к моменту равновесия у образовавшихся веществ у хлора и трихлорида фосфора к моменту равновесия будут равны:
φ(Cl₂) = φ(PCl₃) = 0,407
5) Далее находим объемную долю у хлорид фосфора(V):
φ(PCl₅) = 1 - (φ(Cl₂) + φ(PCl₃)) = 1 - (0,407 + 0,407) = 1 - 0,814 = 0,186
6) Теперь находим парциальное давление PCl₅, по закону парциальных давлений величина парциального давления компонента газовой смеси пропорциональна его объемной доле:
P(PCl₅) = P(смеси) × φ(PCl₅) = 202,6 кПа × 0,186 = 37,6836 кПа ≈ 37,68 кПа
ответ: P(PCl₅) = 37,68 кПа
Решено от : 
m(FeCI3)=48,75гр
найти m (HCI)?
M(FeCI3)=162,5г/моль
n(FeCI3)=m/M=48,75/162,5=0,3
n(FeCI3)=0,3моль
HCI по уравнению в 3 раза больше:
n(HCI)=0,3*3=0,9моль
M(HCI)=36,5г/моль
m(HCI)=n*M=35,5*0,9=32,85гр
m(ра-ра)HCI=32,85/0,1=328,5гр