1. знаходимо масу води за формулою:
m(води)=v(води)•ρ(води), де густина води ρ(води)=1г/мл.
m(води) = 200 мл • 1 г/мл = 200 г. бачимо, що для води об'єм відповідає масі, тому ця дія не є обов'язковою.
2. знаходимо масу речовини (магній сульфату mgso4) за формулою:
m1(речовини)=(m1(розчину)/100 %)•w1(речовини)=
=(300 г/100%) •15%=45 г.
3. знаходимо масу нового розчину:
m(розчину)=m1(розчину)+m(води)=300 г+200г=500г.
4. знаходимо масову частку речовини (магній сульфату mgso4)) в новому розчині за формулою:
w(речовини)=(m1(речовини)/m(розчину))•100 %.
w(речовини)=(45 г/500 г)•100%=9%.
відповідь: w(речовини)=9%.
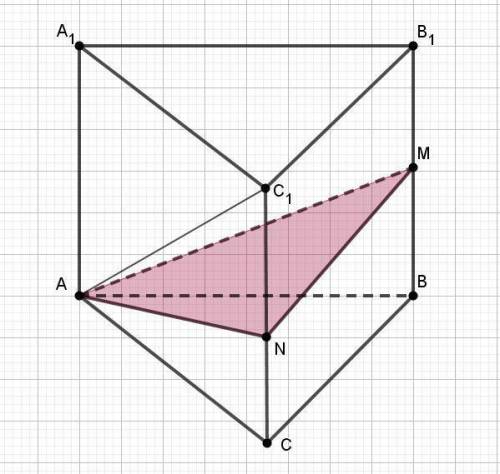
1) Сечение строится по заданным точкам.
Точку N находим в соответствии со свойством биссектрисы (см. пункт 2). Ребро СС1 точкой N делится в отношении 3:5.
2) По заданию AN является биссектрисой угла CAC1.
Диагональ АС1 боковой грани по Пифагору равна √(6² + 8²) = 10.
Примем СN = х.
По свойству биссектрисы х/6 = (8 - х)/10. Сократим знаменатели на 2.
24 - 3х = 5х,
8х = 24,
х = 24/8 = 3.
По заданию ВМ = 8/2 = 4.
Сечение AMN от призмы отсекает пирамиду с основанием BCNM, которое является трапецией (CN ║BM).
S(BCNM) =((3+4)/2)*6 = 21 кв.ед.
Высота H этой пирамиды равна высоте основания АВС.
H = 6*cos 30° = 6*√3/2 = 3√3.
V1 = V(ABCNM) = (1/3)*21*3√3 = 21√3 куб.ед.
Площадь основания призмы So = 6²√3/4 = 9√3 кв.ед.
Объём призмы V = 9√3*8 = 72√3 куб.ед.
Объём отсечённой части призмы равен V2 = 72√3 - 21√3 = 51√3 куб.ед.
ОтношениеV1/V2 = 21√3/51√3 = 7/17.
Объяснение:
Катион и анион не указаны, так что напишу свои:
Ag⁺+Cl⁻=AgCl↓ (белый творожистый осадок)
Al⁺³+3OH⁻=Al(OH)₃↓ (белый студенистый осадок)
№2
5KBr+KBrO₃+3H₂SO₄=3Br₂+3H₂O+3K₂SO₄
2Br⁻-2e=Br₂⁰ 5 восстановитель
2Br⁺⁵+10e=Br₂⁰ 1 окислитель
№3
1) Уксусная кислота CH₃COOH
2) Этанол C₂H₅OH
3) Перманганат калия KMnO₄
4) Раствор хлорида железа FeCl₃
5) Раствор сульфата меди CuSO₄
Вообще можно последние три вещества распознать по цвету раствору
3) KMnO₄ - от розового до фиолетового
4) FeCl₃ - желтый
5) CuSO₄ - голубой
А первые два по запаху.
Но вообще вот реакции:
1) CH₃COOH+NaHCO₃=CH₃COONa+H₂O+CO₂↑ (выделение газа без цвета и запаха)
2) C₂H₅OH+CuO=CH₃CHO+Cu↓+H₂O (выпадает осадок красного цвета)
3) 3K2SO3+2KMnO4 +H2O=3K2SO4+2MnO2↓+2KOH (выпадает осадок тёмно-коричневого цвета)
4) FeCl₃+3NaOH=3NaCl+Fe(OH)₃↓ (выпадает осадок коричневого цвета)
5) CuSO₄+2NaOH=Na₂SO₄+Cu(OH)₂↓ (выпадает осадок голубого цвета)