Объяснение:
1) Назвать вещества:
А) СН3-СН(СН3)-СН=СН2 3-метилбутен-1
Б) СН3-СН3 - этан
2) Составить структурные формулы:
А) Хлоруксусная кислота Cl-СН2 - СООН
Б) Формальдегид H- C = O
I
H
В) Ацетилен HC≡CH
3) Определить объем кислорода, необходимого для сгорания 7,4г этанола
C2H6O + 3O2 = 2CO2 + 3H2O
Молярная масса этанола равна 46 г/моль и 7,4 г этанола соответствуют 0,16 моль. Тогда кислорода будет затрачено на сгорание в 3 раза больше или 0,48 моль. Объем кислорода составит
22,4 л/моль × 0,48 моль = 10,8 л
Карбоновые кислоты - органические вещества, которые имеют в своём составе карбоксильную группу (-СООН)(1 или несколько) с общей формулой R-COOH, где R - алкильный заместитель.
Классифицировать можно по количеству основ(т.е. карбоксильных групп): 1-, 2- и многоосновные.
По силе (средней силы и слабые).
По насыщенности (предельные, непредельные).
Так же они могут быть циклическими и нециклическими.
Только муравьиная кислота применяется в качестве окислителя благодаря одной особенности - а именно отсутствию электрондонорных заместителей(исключая тот единственный фрагмент -СН3), которые ослабляют кислотные свойства, в следствии смещения электронной густоты от себя.(такими могут быть -СН3, -С2Н5 и т д.).
Всё остальное на листочке:
*Ме - какой-то металл в соли,
[О] - окислитель.
У метилэтилового эфира изомеры пропанол-1 и пропанол-2. Они не влезли просто.
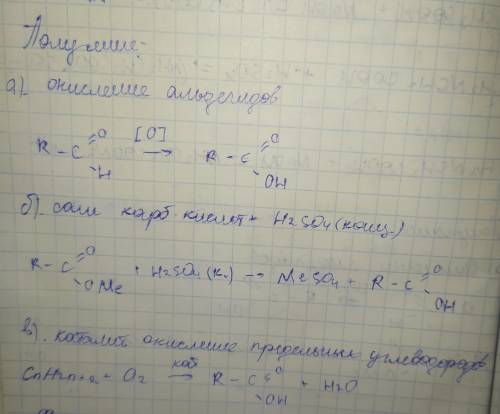




1 1
либо 2) 2NaOH + CO₂ --> Na₂CO₃ + H₂O
2 1
n(CO₂)= 0.88/(12+16*2)= 0.02 моль
m(NaOH)= 5*20%/100%= 1 г
n(NaOH)= 1/(23+16+1)= 0.025 моль
n(NaOH): n(CO₂) = 0.025 : 0.02 = 1.25:1 ==>
Сначала будет протекать р-ия 1 с образованием кислой соли NaHCO₃ (n=0.02 моль), при этом часть NaOH останется (0,025-0,02= 0,005 моль). И далее будет протекать р-ия: NaHCO₃ + NaOH --> Na₂CO₃ + H₂O.
n(Na₂CO₃)= n(NaOH ост.)=0,005 моль, и останется 0.02-0.005 = 0.015 моль NaHCO₃.
m(Na₂CO₃)= 0.005*(23*2+12+16*3)= 0.53 г
m(NaHCO₃)= 0.015*(23+1+12+16*3)= 1.26 г