Химическое равновесие сдвигается согласно принципов Ле-Шателье. Сдвинуть равновесие реакции можно , изменяя температуру(если есть температурный эффект-поглощение или выделение тепла), изменением концентрации исходных веществ или продуктов реакции и изменением давления(для газов). В данном уравнении нужно повысить концентрацию NO и Cl2, снизить концентрацию NOCl, снизить температуру(т,к, это экзотермическая реакция) и повысить давление.
правила такие: при повышении температуры равновесие сдвигается в сторону эндотермической реакции(с поглощением тепла).При повышении давления-в сторону меньшего объема(считаем по коэффициентам до и после реакции).Повышение концентрации исходных веществ смещает равновесие в сторону образования продуктов и наоборот-понижение-в сторону исходных.
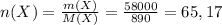 моль
моль
Cu(OH)2 = CuO + H2O
ZnCl2 + 4NaOH = Na2[Zn(OH)4] + 2NaCl
n(CuO) = 2 : 80 = 0,025 моль
n(CuCl2) = n(CuO) = 2 : 80= 0,025 моль
m(CuCl2) = 0,025 *135 = 3,375 г
w(CuCl2) = 3,375 / 6,15 = 0,55, или 55%
w(ZnCl2) = 100-55=45%