m(C₆H₅NH₂)=186г.
Объяснение:
Дано:
m(C₆H₅NO₂)=250г.
------------------------------
m(C₆H₅NH₂)-?
Рішення:
1. Визначимо молярну масу нітробензену :
M(C₆H₅NO₂)=6×12+5+14+2×16=123г./моль
2. Визначимо кількість речовини нітробензену в 250г. :
n₁(C₆H₅NO₂)=m(C₆H₅NO₂)÷M(C₆H₅NO₂)
n₁(C₆H₅NO₂)=250г.÷123г./моль=2моль
3. Запишемо рівняння реакції:
C₆H₅NO₂ + 3H₂ → C₆H₅NH₂ + 2H₂O.
а) за рівнянням реакції кількість речовини:
n(C₆H₅NO₂)=1моль n(C₆H₅NH₂)=1моль
б) за умовою задачі кількість речовини:
n₁(C₆H₅NO₂)=2моль n₁(C₆H₅NH₂)=2моль
4. Визначимо молярну масу анілін :
M(C₆H₅NH₂)=6×12+5+14+2=93г./моль
5. Визначимо масу анілін кількістю речовини 2моль:
m(C₆H₅NH₂)=n₁(C₆H₅NH₂)×M(C₆H₅NH₂)=2моль ×93г./моль=186г.
6. Відповідь: при відновленні нітробензену масою 250г. отримали 186г. аніліну.
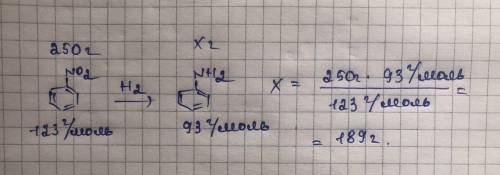
2.оксид углерода(IV) кислотный оксид и он взаимодействует с кислотами:
CO₂+2NaOH = Na₂CO₃ + H₂O реакция обмена
(CO₂)⁰+2Na⁺OH⁻ = Na₂⁺CO₃⁻² + (H₂O)⁰
3.Алюминий в ряду напряжения металлов стоит левее водорода, значит он будет взаимодействовать с кислотами:
2Al+6HCl=2AICI₃ +3H₂↑реакция окислительно-восстановительная
Al⁰+6H⁺Cl⁻=AI⁺³CI₃⁻ +H₂⁰↑
Алюминий восстановитель, а ион водорода окислитель
4. Оксид алюминия амфотерный оксид он будет взаимодействовать как с кислотами так и со щелочами:
Al₂O₃+HNO₃=AI(NO₃)₃ + H₂O реакция обмена
(Al₂O₃)⁰+6H⁺NO₃⁻ = 2AI⁺³(NO₃)₃⁻ + 3(H₂O)⁰
5. Оксид свинца(ll) проявляет амфотерные свойства, реагирует с кислотными оксидами и щелочными оксидами:
PbO+Na₂O = Na₂PbO₂ реакция соединения
(PbO)⁰+(Na₂O)⁰ = Na₂⁺PbO₂⁻
6. Кислоты взаимодействуют с солями
2HNO₃+MgCO₃= Mg(NO₃)₂ +CO₂↑ +H₂O реакция ионного обмена
2H⁺ + 2NO₃⁻ +MgCO₃= Mg²⁺ +2NO₃⁻ +CO₂↑ +H₂O
2H⁺ +MgCO₃= Mg²⁺ + CO₂↑ +H₂O
7. Оксид ванадия(V) проявляет амфотерные свойства, реагирует с кислотными оксидами и щелочными оксидами, :
V₂O₃+FeO≠ не взаимодействует
8. Основной хлорид железа -соль взаимодействует с кислотами:
FeOHCl+HCl= FeCI₂ + H₂O реакция ионного обмена
FeOH⁺ + Cl⁻+ H⁺ + Cl⁻ = Fe²⁺ + 2CI⁻ + H₂O
FeOH⁺ + H⁺ = Fe²⁺ + H₂O