Судя по продуктам реакции, горит углеводород с общей формулой СyHz.
По уравнению реакции:
(1) n(CO2) : n(X) = y : 1
(2) n(H2O) : n(X) = z : 2
n(H2O) = m(H2O) / M(H2O) = 12,6 г / 18 г/моль = 0,7 моль
n(CO2) = V(CO2) / Vm = 13,44 л / 22,4 л/моль = 0,6 моль
М(Х) = Д * М(СН4) = 5,375 * 16 г/моль = 86 г/моль
n(X) = m(X) / M(X) = 8,6 г / 86 г/моль = 0,1 моль
Из пропорций:
(1) y = 0,6/0,1 = 6
(2) z = 2*0,7/0,1 = 14
Общая формула: С6Н14 (гексан)
Проверим баланс по молярной массе:
6*12 + 14*1 = 86 (г/моль)
ответ: С6Н14 — гексан
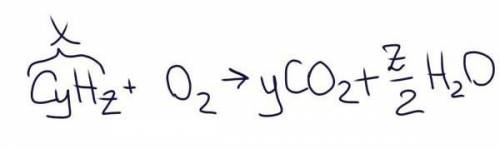
Водород — бесцветный нетоксичный газ без запаха и вкуса. Молекула водорода не полярна. Поэтому силы межмолекулярного взаимодействия в газообразном водороде малы. Это проявляется в низких температурах кипения (-252,6 0С) и плавления (-259,2 0С).
Водород легче воздуха, D (по воздуху) = 0,069; незначительно растворяется в воде (в 100 объемах H2O растворяется 2 объема H2). Поэтому водород при его получении в лаборатории можно собирать методами вытеснения воздуха или воды.
Как его собирают?Цинк вытесняет водород из кислот, как и все металлы, стоящие в ряду напряжений левее водорода. Чтобы собрать водород в пробирку, нужно перевернуть ее вверх дном, потому что водород – легче воздуха и стремится вверх.