Пускай масса кислорода равна х г.
Тогда масса искомого элемента равна (х + 87,5) г.
Зная, что их сумма равна 175 г, составим уравнение:
х + (х + 87,5) = 175;
х + х + 87,5 = 175;
2х + 87,5 = 175;
2х = 175 - 87,5;
2х = 87,5;
х = 43,75 (г) — масса кислорода в оксиде.
Найдем молярную массу кислорода:
M (O₂) = 2 ∙ Ar(O) = 2 ∙ 16 = 32 (г/моль).
Значит, масса кислорода в 1 моле оксида равна 32 г.
Масса кислорода в n моль оксида равна 43,75 г.
Составим пропорцию и выразим из нее количество вещества ХО₂:
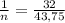 ;
;
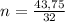 ;
;
 (моль).
(моль).
Судя по формуле соединения, 1 моль оксида содержит 1 моль неизвестного элемента, то есть n (ХО₂) = n (Х).
Формула количества вещества:
n = m : M.
Отсюда выразим молярную массу:
M = m : n.
Масса искомого элемента равна m (O₂) + 87,5 = 43,75 + 87,5 = 131,25 (г).
M (X) = m (X) : n (X) = 131,25 : 1,37 = 96 (г/моль).
Смотрим в таблице Менделеева, какой элемент имеет такую атомную массу, и это молибден (Mo). Это и есть элемент, образовавший данный оксид.
ответ: молибден (Mo).
Алюминий активно вступает в реакцию с разбавленными кислотами: серной, соляной и азотной, с образованием соответствующих солей: сернокислого алюминия Al2SO4, хлорида алюминия AlCl3 и нитрата алюминия Al(NО3)3.
Реакции алюминия с разбавленными кислотами:
2Al + 3H2SO4 —> Al2(SO4)3 + 3H2
2Al + 6HCl —> 2AlCl3 + 3H2
2Al + 6HNO3 —> 2Al(NO3)3 + 3H2
С концентрированными серной и соляной кислотами при комнатной температуре не взаимодействует, при нагревании реагирует с образованием соли, окислов и воды.