BaCO3+2HCl=BaCl2+H2O+CO2
Na2CO3+2HCl=2NaCl+H2O+CO2
BaCl2+Na2SO4=BaSO4(осадок)+2NaCl
в осадок в результате обработки избытком сульфата натрия выпадает сульфат бария (идет только реакция с хлоридом бария, реакция с хлоридом натрия не идет)...
количество вещества сульфата бария, выпавшего в осадок: m(BaSO4)/M(BaSO4)=(46.6г)/(233г/моль)=0,2 моль
карбоната бария было также 0,2 моль...
зная количество вещества и молярную массу карбоната бария (197 г/моль), находим массу карбоната бария: 0,2*197=39,4 г.
теперь находим долю карбоната бария в его смеси с карбонатом натрия:
m(BaCO3)*100%/(m(BaCO3)+m(Na2CO3))=39.4*100/50=78.8%
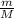
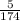 ≈0,0287 моль
≈0,0287 моль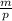 , где p(читается ро) - это плотность раствора.
, где p(читается ро) - это плотность раствора.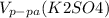 =
=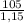 ≈91.3 мл. = 0,0913 л
≈91.3 мл. = 0,0913 л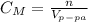
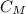 =
= 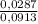 моль/л ≈ 0,314 моль/л
моль/л ≈ 0,314 моль/л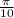 моль/л.
моль/л.
ответ: 3.16*10²⁴ атомов
Объяснение:
N=n*Na
Mr(Fe2(HPO4)3)=400 г/моль
n=140/400 = 0,35
N(Fe)=0.35*6.02*10²³ * 2 = 4.214*10²³ атомов
N(H) = 0.35*6.02*10²³ * 3 = 1.05*10²³ атомов
N(P) = 0.35*6.02*10²³ * 3 = 1.05*10²³ атомов
N(O) = 0.35*6.02*10²³ * 12 = 2.53*10²⁴ атомов
∑N = (4.214+1.05+1.05+25.3)*10²⁴ = 3.16*10²⁴ атомов
ответ: 3.16*10²⁴ атомов