Дано:
m(NaOH) = 4 гр
m(H₂O) = 1 л = 1000 гр
ρ(р-ра NaOH) = 1,2 гр/см³ = 1200 гр/л
-----------------------------------------------------------
Найти:
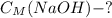
1) Для начала мы найдем массу раствора NaOH:
m(р-ра NaOH) = m(NaOH) + m(H₂O) = 4 гр + 1000 гр = 1004 гр
2) Далее находим объем раствора NaOH:
V(р-ра NaOH) = m(р-ра NaOH)/ρ(р-ра NaOH) = 1004 гр/1200 гр/л ≈ 0,8367 л ≈ 0,84 л
3) Потом мы находим количества вещества у NaOH:
M(NaOH) = 23+16+1 = 40 гр/моль
n(NaOH) = m(NaOH)/M(NaOH) = 4 гр/40 гр/моль = 0,1 моль
4) Потом мы находим молярную концентрацию раствора NaOH:
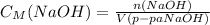 - молярную концентрацию раствора NaOH
- молярную концентрацию раствора NaOH
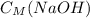 = 0,1 моль/0,84 л ≈ 0,119 моль/л ≈ 0,12 моль/л
= 0,1 моль/0,84 л ≈ 0,119 моль/л ≈ 0,12 моль/л
ответ: 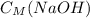 = 0,12 моль/л
= 0,12 моль/л
Cu + H2SO4(конц)= CuSO4 + SO2↑ + H2O
Cu(0) + H(+1)2S(+6)O(-2)4(конц.) → Cu(+2)S(+6)O(-2)4 + H(+1)2O(-2) + S(+4)O(-2)2↑
Cu(0) - 2e -> Cu(+2) окиснення відновник
S(+6) + 2e -> S(+4) відновлення окисник
Cu(0) + S(+6) -> Cu(+2) + S(+4)
Cu + 2H2SO4 = CuSO4 + SO2↑ + 2H2O
S + H2SO4(конц.) = SO↑2 + H2O
S(0) + H(+1)2S(+6)O(-2)4 = S(+4)O(-2)2↑ + H(+1)2O(-2)
2 H2SO4 + S → 3 SO2 ↑ + 2 H2O
Это окислительно-восстановительная реакция:
S(0) - 4 e- → S(+4) (окисление)
2 S(6+) + 4 e- → 2 S(+4) (восстановле́ние)
S является восстановителем, H2SO4 является окислителем.
(...)- коефіцієнти окислення, пишуться зверху біля хімічних елементів
Объяснение:
v(CO2)=5,6л
w(NaOH)=6%
Найти:m(NaOH)-?
РЕШЕНИЕ:
2NaOH+CO2=Na2CO3+H2O
V(не объем,а количество вещества,то есть ню)
ню(CO2)=5,6/22,4=0,25 моль
ню(CO2)=2ню(NaOH) следовательно
ню(NaOH)= 2*0,25=0,5 моль
m(NaOH)=0,5*40=20г
ответ:20г
вроде такое решение