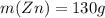
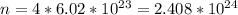
Объяснение:
Уравнение взаимодействия цинка с соляной кислотой выглядит следующим образом:

Так как водорода выделяется 44.8 л (1 л = 1 дм³), то количество вещества водорода равно 44.8 / 22.4 = 2 моль
По уравнению количество вещества водорода совпадает с количеством вещества цинка, т.е. ν(Zn) = 2 моль, а учитывая что молярная масса цинка равна 65 г/моль, то масса прореагировавшего цинка равна 65 * 2 = 130 г.
Количество вещества прореагировавшей кислоты в 2 раза больше чем количество вещества водорода, т.е. составляет 4 моль. Чтобы найти количество молекул кислоты, надо это количество вещества умножить на постоянную Авогадро.
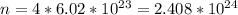
V=16,44 мл
Объяснение:
Запишем уравнение реакции:
НCl+NaOН=NaCl +Н2О
Вычислим молярные массы соляной кислоты и гидроксида натрия
Mr(НCl)=1+35,5=36,5 г/моль
Mr(NaOН)=23+1+16=40 г/моль
Вычислим количество вещества гидроксида калия:
n(NaOН)=m(NaOН)/Mr(NaOН)=4/40=0,10 моль
По уравнению реакции, так как перед кислотой и щелочью стоят коэффициенты 1 следует, что оба вещества взаимодействуют в молярном соотношении 1:1, следовательно, соляной кислоты нужно тоже взять 0,1 моль.
Вычислим массу взятой соляной кислоты:
m(НCl)=n(НCl)*Mr(НCl)=36,5*0,1=3,65 грамм
Вычислим массу 20% раствора соляной кислоты, которую нужно взять:
3,65 грамм составляет 20%
Х грамм составляет 100%
Отсюда Х=3,65*100/20=18,25 грамма
Вычислим объем раствора по формуле:
V=m/p=18,25/1,11=16,44 мл
N₂ + 3H₂ = 2NH₃ (аммиак) '
условия: (Kt, t-500C, P=2·10⁴кПа)