Составим цепочку превращений:
С2Н6 – С2Н4 – (-Н2С-СН2-)n
Запишем уравнения:
Н3С - СН3 = Н2 + Н2С = СН2 – реакция дегидрогенизации, получен этилен;
nH2C = CH2 = (- H2C - CH2 -)n – реакция полимеризации происходит при нагревании под давлением, в присутствии катализатора, образуется полиэтилен.
Приведенные уравнения показывают связь алканов, алкенов и высокомолекулярных соединений, а также возможности получения полимера из этана. Полиэтилен применяется в электротехнике как изоляционный материал и в быту для упаковки.
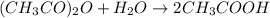
Задача №1
Для решения такой задачки, воспользуемся формулой:
Получаем:
ответ6 скорость реакции возрастет в 243 раза(не хило)
Задача №2
Запишем уравнение:
- Запишем кинетическое уравнение для данной реакции:
Пусть
Запишем кинетическое выражение реакций до увеличения давления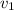 и после
и после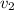 :
:
Теперь разделим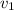 на
на 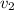
Сокращаем и получаем, что скорость реакции возрасла в 9 раз
ответ: скорость реакции возрастет в 9 раз(тут вроде более менее:DD)
Задание №3
Увеличивая концентрацию угарного газа мы смещаем равновесие в сторону продуктов реакции т.е. ->
Уменьшая температуру, мы смещаем равновесие в сторону продуктов реакции, т.е. ->
Увеличение давления сместит равновесие в сторону продуктов реакции, т.е. ->, т.к. число моль газов в правой части меньше, чем число моль газов в левой части
Вот так))