Составим уравнение реакции:
C2H5OH + 3O2 = 3H2O + 2CO2
Посчитаем молярные массы веществ:
а) C2H5OH
12*2 + 1*5 + 16 + 1 = 46 г/моль
б) H2O
2*1 + 16 = 18 г/моль.
Т. к. в реакции учавствуют 3 моль воды, то 18*3 = 54 г .
Исходя из уравнения в реакции учавствуют 3 моль О2 и 2 моль СО2, следовательно,
используя число Авогадро 22,4 л/моль считаем объемы газов V(O2) = 3 * 22.4 = 67.2 л;
V(CO2) = 2 * 22.4 = 44.8 л/
Составляем пропорции:
m(H2O) = 54 * 420 / 46 = 493 (г).
V(CO2) = 44.8 * 420 / 46 = 409 (л).
V(O2) = 67.2 * 420 / 46 = 614 (л).
Так, сначала я расскажу как я решал задачу, а потом оформление:
Сначала введем обозначения:
Исходное состояние.
Рассчитаем массу соли в исходном растворе.
Смешиваем.
Мы добавили к первоначальному растовру 20 грамм соли - значит мы увеличили массу раствора на 20грамм, т.е. масса получившегося раствора равна: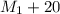 г = 350г+20г = 370грамм
г = 350г+20г = 370грамм
Но, добавив 20 грамм соли к раствору, мы увеличили не только массу арствора, но и массу соли которая есть в растворе, масса соли в получившемся растворе -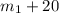 грамм = 72,5 грамм.
грамм = 72,5 грамм.
Теперь у нас есть все, чтобы рассчитать массовую долю соли в получившемся растворе:
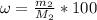 = 72,5г/370г*100% = 19,6%
= 72,5г/370г*100% = 19,6%
Теперь оформление:
Дано:
масса добавленной соли = 20 грамм.
Найти:
Рассчитаем массу соли в растворе:
Рассчитаем массу получившегося расвтора:
Рассчитаем массу соли в получившемся растворе:
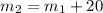 г = 52,5г + 20г = 72,5
г = 52,5г + 20г = 72,5
Рассчитываем массовую долю:
ответе: массовая доля соли = 19,6%(или0,196)