а) Это запись для атомов одного и того же хим элемента (ответ А)
b) элемент - Кислород, О.
с) см. ниже
Объяснение:
Проясню, что обозначают верхний и нижний индексы в приведенной записи:
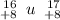
• верхний индекс — массовое число атома элемента
Определяет массу атома, т.е. суммарное количество протонов и нейтронов в ядре атома
• нижний индекс — заряд ядра атома элемента.
Обозначает количество протонов в ядре, также этот индекс указывает порядковый номер элемента в Периодической таблице Менделеева (т.к. количество протонов в ядре элемента равно количеству электронов на орбиталях, а именно электроны на орбиталях и определяют в большой степени химические свойства элементов)
В нашем случае равные нижние индексы (+8).
Следовательно, в обеих записях указаны атомы для одного и того же хим. элемента. Причем порядковый номер элемента равен 8.
8-й элемент - это Кислород, О.
А приведенные записи относятся к атомам О, но с разными атомными массами (у кислорода в ядре 8 протонов и чаще всего 8 нейтронов, но может содержаться и 7, и 9 нейтронов, что дает нам разные атомные массы)
Атомы одного и того же элемента, имеющие разные массы называются изотопами.
В нашем случае приведены записи двух изотопов кислорода (условно называемые кислород-16 и кислород-17)
2FeCl2 + Cl2 = 2FeCl3
14HCl + K2Cr2O7 = 3Cl2 + 2CrCl3 + 2KCl + 7H2O
Из первого УХР видно, что Cl нужен в количестве 1 моль, следовательно и во втором уравнении хлора так же 1 моль
Находим массу хромата калия.
n(K2Cr2O7) = 1 моль/3 = 0,33 моль
m(K2Cr2O7) = 0,33 моль * 294 г/моль = 97,02 г
n(HCl) = 14 моль / 3=4,67 моль
m(HCl) = 4,67 моль * 36,5 г/моль = 170,455 г (это масса растворимого вещества HCl, находим массу и объем раствора).
m(раствора)=170,455 г * 100%/35,2% =484,25 г
V=m/p
V(HCl) = 484,25 г/ 1,175 г/мл = 412,13 мл