1) H₂SO₄
Степень окисления H +1; степень окисления S +6; степень окисления О -2.
2) SO₃
Степень окисления S +6; степень окисления O -2.
3) SO₂
Степень окисления S +4; cтепень окисления O -2.
4) H₂S
Cтепень окисления H +1; cтепень окисления S -2.
5) CS₂
Cтепень окисления C +4; cтепень окисления S -2.
6) H₂SO₃
Cтепень окисления H +1; cтепень окисления S +4; cтепень окисления O -2.
7) K₂SO₄
Cтепень окисления K +1; cтепень окисления S +6; cтепень окисления O -2.
8) Al₂(SO₄)₃
Cтепень окисления Al +3; cтепень окисления S +6; cтепень окисления O -2.
Объяснение:
Уравнение Клапейрона-Менделеева.
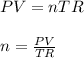
где n – число молей газа;
P – давление газа (например, в атм;
V – объем газа (в литрах);
T – температура газа (в кельвинах);
R – газовая постоянная (0,0821 л·атм/моль·K).
n=(1.02*1.56):(300.15*0,0821)=1.5912:24.6423=0.0646моль
M= m:n=2.86/0.0646=44.29г/моль
Как перевести атмосферу в паскали?
1 атм = 101325 Па = 101,325 кПа.
1,037 * 10^5= 1.02атм
Как перевести градусы в К?
Расчет происходит по формуле: T=t+273=27+273.15=300.15K,
где T— температура в кельвинах, t — температура в градусах Цельсия
Составим пропорцию, чтобы найти массу нового раствора
100 г - 0,15
x г - 0,3 (массовая доля увеличилась в два раза)
По основному свойству пропорции:
x = = 200 г
m(H2SeO4) = 200 - 100 = 100 г (именно столько селеновой кислоты должно было образоваться после добавления к имеющемуся раствору гидроксида. Т.е. это масса кислоты из уравнения реакции выше)
n(H2SeO4) = m/M = 100/145 = 0,67 моль
n(H2SeO4) : n(SeO3) = 1 : 1 (см. цифры перед формулами веществ в уравнении реакции)
n(SeO3) = 0,67 моль
m(SeO3) = M*n = 127*0,67 = 85 г
ответ: 85 г