№14. комплексные соли: 1) продукт полного замещения атомов водорода в кислоте на атомы металла 2) продукт неполного замещения атомов водорода в кислоте на металл 3) продукты неполного замещения гидроксогрупп в основании на кислотный остаток 4) вещества, образующиеся в результате взаимодействия амфотерных оксидов и гидроксидов № 15. арсин: 1) siн4 2) рн3 3) ash3 4) в2н6 № 16. изотопы элементов отличаются: 1) количеством нейтронов 2) атомным номером 3) количеством валентных электронов 4) количеством протонов № 17. элемент – это: 1) электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов 2) наименьшая частица вещества, его свойствами 3) определённый вид атомов с одинаковым положительным зарядом ядра 4) из одного элемента образуются несколько простых веществ № 18. радиус атомов в группе: 1) уменьшается 2) увеличивается 3) остаётся постоянным 4) периодически изменяется № 19. вещества с атомной кристаллической решёткой: 1) белки, днк 2) алмаз, кварц 3) вода, йод, углекислый газ 4) соли, гидроксиды, органические основания № 20. золи: 1) водные растворы неэлектролитов 2) водные растворы слабых электролитов 3) водные растворы сильных электролитов 4) коллоидные растворы № 21. гидраты – это: 1) ионы, связанные с молекулами воды 2) растворимые соли 3) нерастворимые соли 4) катионы и анионы электролита № 22. пример катализатора: 1) катионы са²⁺ 2) mno2 3) глицерин 4) соединение серы, мышьяка и ртути № 23. металлы вытесняют водород из растворов кислот если: 1) находятся правее водорода в ряду 2) находятся левее водорода в ряду 3) находятся в начале ряда 4) находятся в конце ряда № 24. силан: 1) siн4 2) рн3 3) ash3 4) в2н6 № 25. взаимодействие кислоты с металлами: 1) нcl → h⁺ + cl ¯ 2) ch3cooh + mg→ (ch3coo)2mg + h2 3) cao + hno3→ cano3 + h2o 4) zno + 2ch3cooh → (ch3coo)2zn + h2o № 26. кислая соль: 1) nacl 2) мg(hso4) 2 3) (сuoh)2co3 4) na[al(oh)4] № 27. степень диссоциации сильных электролитов: 1) α=0 2) α ˃ 30% и стремиться к 1 3) α ˂ 3%, 4) α=5 № 28. диссоциация средних солей: 1) na2co3 → 2na⁺ + co3²‾ 2) nahсo3 = na⁺ + hсo3 ‾ 3) alohcl2 → aloh²⁺ + 2cl‾ 4) na2[zn(oh)4] → 2na⁺ + [zn(oh)4] ²‾ № 29. несолеобразующий оксид: 1) mgо 2) so3 3) na2o 4) co № 30. фенолфталеин в щелочной среде: 1) синий 2) розовый 3) малиново-фиолетовый 4) прозрачный
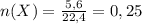 моль
моль
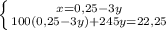
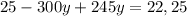

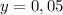
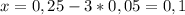
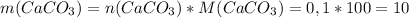 г
г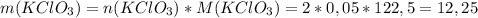 г
г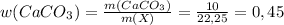 или 45%
или 45% или 55%
или 55%
15. 3
16. 1
17. 1
18. 2 (по движению сверху вниз)
19. 2
20. 3
21. 1
22. 2
23. 2
24. 1
25. 2
26. 2
27.2
28. 1
29. 4
30. 3