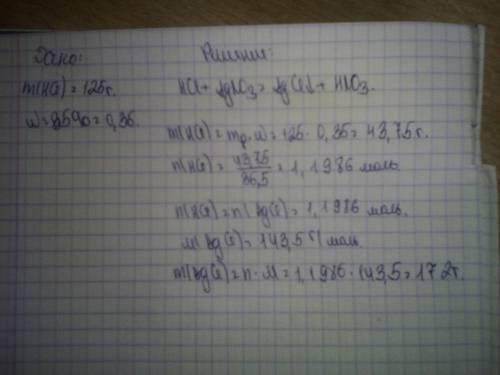
этого термина существуют и другие значения, см. Нейтрализация (значения).
Реакция нейтрализации между гидроксидом натрия и соляной кислотой. Индикаторный агент бромтимоловый синий
Реакция нейтрализа́ции (от лат. neuter — ни тот, ни другой) — реакция взаимодействия кислоты и основания между собой с образованием соли и слабо диссоциирующего вещества (воды).
В большинстве своем, реакции нейтрализации экзотермичны. К примеру, реакция гидроксида натрия и соляной кислоты:
{\displaystyle {\mathsf {HCl+NaOH\rightarrow NaCl+H_{2}O}}}{\mathsf {HCl+NaOH\rightarrow NaCl+H_{2}O}}
В сокращенном ионном виде уравнение записывают так:
{\displaystyle {\mathsf {H^{+}+OH^{-}\rightarrow H_{2}O}}}{\displaystyle {\mathsf {H^{+}+OH^{-}\rightarrow H_{2}O}}}
Тем не менее, существуют также и эндотермические реакции нейтрализации, например, реакция гидрокарбоната натрия (пищевой соды) и уксусной кислоты.
К понятию нейтрализации также могут относиться реакции сильной кислоты с карбонатами, так как в результате такой реакции получается соль и угольная кислота, которая относится к слабым кислотам (не создает полноценную кислотную среду, не вступает в реакции и слабо диссоциирует), а также к нестабильным, поэтому разлагается на углекислый газ и воду — два нейтральных вещества (оксида).
Содержание
1 Примеры
2 Применение
3 См. также
4 Примечания
Объяснение:
Надеюсь так если нет пиши
2 HCl+CuO = CuCl2 + H2O - хлорид меди 2, вода (обмена);
CuCl2 + NaOH = Cu(OH)2 + NaCl - гидроксид меди 2, поваренная соль (обмена);
Cu(OH)2 = CuO + H2O - оксид меди 2, вода (разложения);
4 Fe + 3 O2 = 2 Fe2O3 - оксид железа 3 (соединения);
Fe2O3 + 3 H2SO4 = Fe2(SO4)3 + 3 H2O - сульфат железа 3, вода (обмена);
Fe2(SO4)3 + 3 BaCl2 = 3 BaSO4 + 2 FeCl3 - сульфат бария 2, хлорид железа 3 (обмена);
S + O2 = SO2 - сернистый газ (соединения);
SO2 + 2 NaOH = Na2SO3 + H2O - сульфит натрия, вода (обмена );
Na2SO3 + Ca = CaSO3 + 2 Na - сульфит кальция 2, натрий (замещения).
АgNO3
mppaHCL)=125g
Wppa(HCL)=35%
найти m(AgCL)-?
Решение
43.75g Xg
AgNO3 + HCL --> AgCL+HNO3
36.5 143.5
1) Определяем массу вещества соляной кислоты
mвва (HCL)=mppa(HCL)*W(HCL) / 100% = 125*35 / 100=43.75g
2) Зная массу вещества соляной кислоты по уравнению реакции находим массу образовавшегося осадка
M(HCL)=36.5 g/mol, M(AgCL)=143.5g/mol
составляем пропорцию и решаем
43.75/36.5 = х/143.5 Х=172г
ответ 172 гр