1.В начале узнаем сколько фосфата кальция участвовало в реакции(75%):
310 кг=310 000 г
310 000г-100%
х г-75%
х=310 000г*75%/100%=232 500 г
2.Теперь напишем уравнение реакции:
Ca3(PO4)2+3H2SO4===>2H3PO4+3CaSO4
Из уравнения реакции можно сделать вывод,что 2v(Ca3(PO4)2)=v(H3PO4) (коэффициенты перед веществами в уравнении реакции)
3.M(Ca3(PO4)2)=40*3+31*2+16*8=310 г/моль
v(Ca3(PO4)2)=m/M=232 500г / 310 г/моль=750 моль
Значит v(H3PO4)=750моль*2=1500 моль
M(H3PO4)=3*1+31+16*4=98г/моль
m(H3PO4)=v*M=1500 моль*98г/моль=147 000г или 147 кг
ответ:m(H3PO4)=147 000г или 147 кг
Уравнения происходящих реакций:
1!Раствор известковой воды содержал или
Осадок -1,0 г СаСОз составляет 1,0/100 = 0,01 (моль) СаСО3.
Предполагаем два варианта решения задачи:
1) Са(ОН)2 - в избытке, тогда на осаждение СаСО3 потребовалось 0,01 моль СО2, т. е. v(CO2) = 0,01 моль, а СnН2n+2 также взято 0,224/22,4 = 0,01 моль, следовательно n=1; СnН2n+2 — метан: СН4;
2) Са(ОН)2 - в недостатке, когда осадок массой 0,1 г является результатом двух реакций - осаждения и частичного растворения по уравнению nСаСО3 + nСО2 + nН2О = nСа(НСО3)2
При осаждении получается 0,02 моль СаСО3, остается 0,01 моль СаСО3, т. е. 0,01 моль СаСО3 вступило в последнюю реакцию. Рассчитаем количество СO2:
а) для осаждения:
kCO2 kCa (OH)2 kCaCO3 v x0,02 моль 0,02 моль;
x = 0,02 моль;
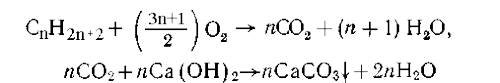
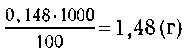
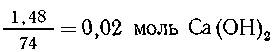
Na2SO4 + Ba(NO3)2 = BaSO4 + 2NaNO3
2Na(+) + SO4(-2) + Ba(+2) + 2NO3(-) = BaSO4 + 2Na(+) + 2NO3(-)
Ba(+2) + SO4(-2) = BaSO4