1)Простые вещества — вещества, состоящие исключительно из атомов одногохимического элемента (из гомоядерных молекул)[1][2], в отличие от сложных веществ.
2)Калий находится под порядковым номер 19, атомная масса равна 39.0938, находится в 1 группе в 4 периоде, имеет 4 энергетических уровня, щелочной металл, при взаимодействия с водой образует щелочь.
3)
1) S+Fe = FeS
2) FeS+2 HCl=FeCl2+H2S
3) 2H2S+3O2=2SO2+2H2O
4) SO2+2 NaOH=Na2SO3+H2O
или
4) SO2+ Na2O=Na2SO3
5) Na2SO3+H2SO4=Na2SO4+H2SO3
или
5) 2 Na2SO3+O2=2Na2SO4
6) Na2SO4+Ba(NO3)2=BaSO4 (осадок) +NaNO3
или
6) Na2SO4+BaCl2=BaSO4 (осадок) +2NaCl
4)Ag+HNO3= AgNO3+NO+H2O
І2+Cl2+H2O--->HIO3+HCl
Окислителем будет хлор Cl2
Восстановитель - йод I2
Коэффициент перед восстановителем: 1 (ответ Б)
определяем степени окисления тех атомов, которые её меняют в ходе реакции:
В соединении I2 - степень окисления йода 0. А после реакции степень окисления йода в соединении HIO3 стала +5, то есть йод отдал (потерял свои электроны (частицы с отрицательным зарядом). Процесс отдачи электронов - окисление. а сам йод - восстановитель.
В соедининии Cl2 степень окисления хлора 0, а после реакции в соединении HCl степень окисления хлора -1. То есть хлор забрал (притянул к себе) электроны. Это процесс восстановления. А сам хлор - окислитель.
Теперь разберемся, сколько именно электронов.
Если йод меняет степень окисления с 0 до +5, то происходит отдача 5 электронов, а т.к. атомов йода 2, то 2*5=10 электронов.
Если хлор меняет степень окисления с 0 до -1, происходит присоединение одного электрона, но т.к. атомов хлора 2, то 2*1=2 электрона.
Чтобы уравнять количества вещ-в уравнении, надо проставить коэффициенты (крест накрест), т.е перед йодом поставим 2, а перед хлохом 10. Но их можно сократить на 2, поэтому перед йодом I2 будет 1, а перед хлором Cl2 будет 5.
Потом уравниваем количества других вещ-в (водорода, потом кислорода). в итоге будет так:
0 0 +5 -1
J2+5Cl2+6H2O=2HJO3+10HCl
коэфф-ты 0 +5
1| 2 I J2 -10е (электронов)=2I - процесс окисления, J восстановитель
0 -1
5I 10 I Cl2 +2e (Электрона)=2Cl - процесс восстановления, Cl окисл-ль
5)Не смог я всего лишь 8 класс сорри
Привет
Начнем с конца.
CuSO4+ 2NaOH = Cu(OH)2 + Na2SO4
m(р-ра) = 48 г
w(р-ра) = 10%
m(CuSO4) = 48×0.1= 4.8 грамм
n(CuSO4) = 4.8/160= 0.03 моль
Так как CuSO4 и NaOH находятся в молярном соотношении 1 к 2, то следует:
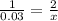
x= 0.06 моль NaOH
При электролизе раствора NaOH выделяется 3 моль газов (2H2 и O2) , но по задаче даётся 134.4 литра
Газы выделяются потому что электролизуется Вода
NaOH не электролизуется
2H2O =(электролиз) 2H2 + O2
При электролизе 2 моль воды, выделятся и улетучивается 3 моль газов, но по задаче даётся 134.4 литра, а это 134.4/22.4 = 6 моль газов
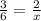
x= 4 моль воды электролизовалось
120×0.1= 12 грамм NaOH
120-12= 108 грамм воды
Так как 72 грамм воды электролизовалось (4×18=72), масса раствора оказалась: 120-72 = 48 грамм
В растворе содержится 12 грамм NaOH
Моль NaOH = 12/40 = 0.3 моль
На осаждение CuSO4 использовали 0.06 моль NaOH
m(NaOH) = 0.06 × 40= 2.4 грамм
Вопрос задачи: Вычислите какую часть (%) раствора использовались для осаждения CuSO4
Масса раствора была 48 грамм - это 100%, 2.4 грамм - X
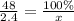
x= 5%
ответ: 5%
Если будут вопросы, отпишитесь в комментариях
V(CO2)=60л*179,2л/44,8л=240л
ответ: 240л