⤵
Объяснение:
Нам уже сказано,что это соль.Соли-сложные вещества,в которых присутствует металл и кислотный остаток,их общая формула:Мет(x).Кислотный ост.(y)
Но каков будет металл и кислотный остаток?Нам известно,что кислота является галогеноводородной,это значит, после водорода в формуле будет стоять элементы из 7-ой группы:хлор,фтор,бром,йод.Но какой же из них?Зная,что при взаимодействии какой-то соли с этой кислотой,мы будем получать белый осадок.Можем предположить,что это будет хлороводородная кислота.И её соль,хлорид серебра нерастворима и имеет белый окрас.Мы узнали кислотный остаток,хлорид.Теперь можем найти и металл,это будет литий,так как он упоминается в задании,в задании,как самый лёгкий, стоит в группе щелочных металлов,которым свойственна химическая активность,и его плотность ниже остальных металлов.И у нас получается формула:LiCl(хлорид лития).
С этой формулой,составляем ионные уравнения:
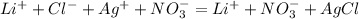
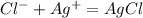
Найменша комірка, яка зберігає усі елементи симетрії кристалу, називається елементарною коміркою.
Навіть у випадку кристалу із одним сортом атомів елементарна комірка містить кілька атомів. Наприклад, кристал заліза має кубічну об'ємноцентровану ґратку із 2 атомами в елементарній комірці. При високих температурах залізо переходить у фазу з ґранецентрованою кубічною ґраткою із 4 атомами в елементарній комірці.
Типи раток
Кристалічні системи
(Сингонія) 14 ґраток Браве
триклінна Triclinic
моноклінна примітивна базоцентрована
Monoclinic, simple Monoclinic, centered
ромбічна примітивна базоцентрована об'ємноцентрована гранецентрована
Orthorhombic, simple Orthorhombic, base-centered Orthorhombic, body-centered Orthorhombic, face-centered
гексагональна Hexagonal
тригональна Rhombohedral
тетрагональна примітивна об'ємноцентрована
Tetragonal, simple Tetragonal, body-centered
кубічна примітивна об'ємноцентрована гранецентрована
Cubic, simple Cubic, body-centered Cubic, face-centered
Основні параметри кристалічних ґраток[1]:
період або параметр ґратки дорівнює довжині ребра ґратки у напрямі головних осей кристалічної ґратки;
координаційне число (К) характеризує щільність пакування ґратки, визначає кількість найближчих і рівновіддалених атомів у певній кристалічній ґратці;
базис — це кількість атомів (іонів), що належать до однієї ґратки;
атомний радіус — це половина відстані між центрами найближчих атомів у кристалічній ґратці певної кристалічної системи;
коефіцієнт компактності — це відношення об'єму, що займають атоми (іони), до всього об'єму ґратки даного типу.
Дефекти кристалічної ґратки
Дефекти кристалічної ґратки. а — незаповнений вузол (вакансія); б — власний атом між вузлами; в — чужорідний атом між вузлами; г — чужорідний атом у вузлі; д — йон з аномальним зарядом.
Розташування структурних елементів у кристалічних ґратках мінералів рідко відповідає цій класичній картині, яка характеризується послідовним розташуванням у ґратці атомів або йонів (так звані ідеальні кристали). На противагу ідеальним кристалам, для яких характерне правильне розташування і періодичність атомів або йонів, реальні кристали відрізняються рядом відхилень — дефектів кристалічної ґратки (дислокацій). Згідно з загальноприйнятою класифікацією, розрізняють такі дефекти кристалічної ґратки (мал.):
пустий вузол, створений внаслідок випадання з ідеальної ґратки атома або йона;
власний атом або йон ґратки, розташований між її вузлами;
чужорідний атом або йон, розташований між вузлами ґратки;
чужорідний атом, який заміщає власний атом ґратки;
йон у ґратці в нормальному стані, але з аномальним зарядом.
Объяснение:
Объяснение:
1. Известно, что это соль
А) которая образованна от сильной кислоты, которая является галогеноводородом и дает соль с серебром имеющую белый цвет
Это соляная кислота (НСl), при взаимодействии с серебром образуется белая, нерастворимая в воде соль AgCl
Б) и гидроксида самого лёгкого металла. Самый лёгкий металл - Li ( первый метал по счёту в таблице Менделеева), его гидроксид - LiОН
Таким образом искомая соль - хлорид лития LiCl ( НСl + LiОН=LiCl+H2O)
2. Напишите полное и сокращенное уравнение реакции этой соли с нитратом серебра.
В результате растворения взаимодействия хлорида лития с нитратом серебра (I) (LiCl + AgNO3 = ?) происходит образование средних солей – хлорида серебра (I) и нитрата калия. Молекулярное уравнение реакции имеет вид:
LiCl + AgNO3 = AgCl + KNO3
Запишем ионные уравнения, учитывая, что хлорид серебра (I) нерастворимое в воде соединение, а значит на ионы не распадается, т.е. не диссоциирует.
Первое уравнение называют полным ионным, а второе – сокращенным ионным.
1) K^{+} + Cl^{-} + Ag^{+} + NO_3^{-} = AgCl + K^{+} + NO_3^{-}
2) Cl^{-} + Ag^{+} = AgCl.