Объяснение:
KMn⁺⁷O₄ + Na₂S⁺⁴O₃ + H₂O → Mn⁺⁴O₂↓ + Na₂S⁺⁶O₄ + KOH
Mn⁺⁷+3e⁻ → Mn⁺⁴ 3 2
6
S⁺⁴-2e⁻ → S⁺⁶ 2 3
Mn⁺⁷ окислитель, процесс восстановления
S⁺⁴ восстановитель, процесс окисления
2KMnO₄ + 3Na₂SO₃ + H₂O = 2MnO₂↓ +3 Na₂SO₄ + 2KOH
KMn⁺⁷O₄ + Na₂S⁺⁴O₃ + КOH → Na₂S⁺⁶O₄ + K₂Mn⁺⁶O₄ + H₂O
Mn⁺⁷+1e⁻ → Mn⁺⁶ 1 2
2
S⁺⁴-2e⁻ → S⁺⁶ 2 1
Mn⁺⁷ окислитель, процесс восстановления
S⁺⁴ восстановитель, процесс окисления
2KMnO₄ + Na₂SO₃ + 2КOH = Na₂SO₄ + 2K₂MnO₄ + H₂O
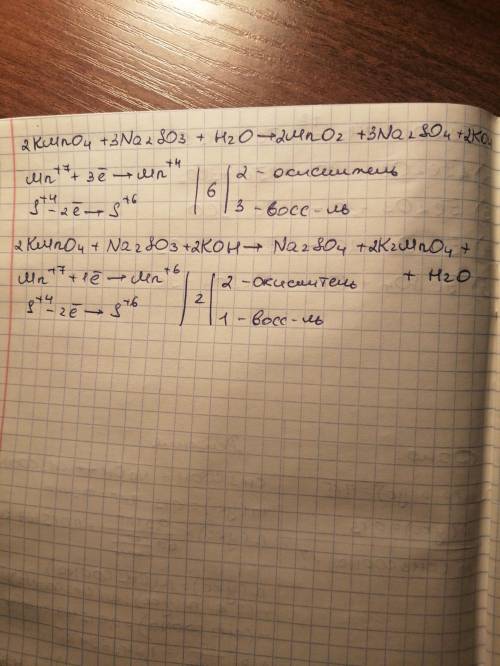
K2SO4 = 2К(-) = SO4(2-)
катод: 2H2O + 2e = H2 + 2OH(-)
анод: 2H2O - 4e = O2 + 4H(+)
2H2O = 2H2+O2
n(O2)при н.у.=V/Vмолярный=11,2л/22,4л/моль=0.5моль
n(О2):n(H2)=1:2
n(Н2)=1моль
Процессы на катоде:
2H2O = H2 + 2OH(-)
n(H2):n(OH)=2:1
n(OH)=2моль
К(+) + ОН(-) = КОН
n(ОН):n(КОН)=1:1
n(КОН)=2моль
m(КОН)=n*M=2моль*56г/моль=112г
ответ: 112 г