4
Объяснение:
Формульная единица — частица или совокупность частиц вещества, представленная его химической формулой, в данном случае ZnS
Посчитаем, сколько формульных единиц находится в одной ячейке
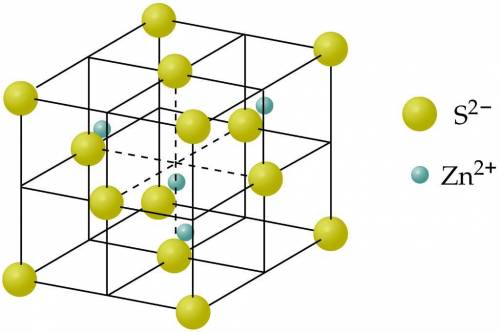
Рассматриваем ионы Zn, они расположены в объеме ячейки, поэтому целиком принадлежат ей, и в 1 ячейке находится 4 иона Zn
Ионы S находящиеся в вершинах, принадлежат сразу 8 ячейкам, поэтому отдельной ячейке принадлежит только 1/8 каждого иона.
Всего у ячейки 8 вершин, и соответственно ей принадлежит еще
(1/8)*8 = 1 ион S
Поскольку решетка гранецентрированная, в центре каждой грани также находится ион S. Ионы в гранях принадлежат сразу 2 ячейкам, значит, данной ячейке принадлежит 1/2 каждого такого иона.
Так как граней 6, то поучаем 6*(1/2)= 3 иона
Итого 1 + 3 = 4 иона S
1 ион Zn и 1 ион S образуют формульную единицу
Значит, всего в ячейке сфалерита 4 формульных единицы
4
Объяснение:
Zn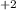 - Кубическая гранецентрированная решетка. Значит число Zn
- Кубическая гранецентрированная решетка. Значит число Zn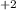 равно 4 (6 атомов на гранях, 8 на вершинах, учитывая коэффициенты пересчёта получаем,
равно 4 (6 атомов на гранях, 8 на вершинах, учитывая коэффициенты пересчёта получаем, 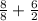 , что и даёт 4)
, что и даёт 4)
Притом, каждый в сфалерите каждый ион цинка тетраэдрически окружен ионами серы, а каждый ион серы — ионами цинка, расположенными по вершинам тетраэдра.
Количество атомов серы на ячейку - также равно 4 (Для того чтобы это заметить достаточно расположить атомы серы в вершины куба, и получится ровно тоже самое - 6 атомов на грани и 8 на вершинах)
Реакции ионного обмена протекают практически до конца в случае образования труднорастворимых или малодиссоциирующих веществ. В данном случае и среди реагентов, и среди продуктов есть малорастворимые вещества - фосфат кальция и фосфат серебра.
Произведения растворимости Ks и растворимости S этих солей:
Ca₃(PO₄)₂ ⇄ 3 Ca²⁺ + 2 PO₄³⁺
Ks = [Ca²⁺]³ * [PO₄³⁺]² = 2,0*10⁻²⁹
S = [Ca²⁺] / 3 = [PO₄³⁺] / 2
[Ca²⁺] = 3S
(потому что при растворении 1 моль фосфата кальция получается 3 моль ионов кальция)
[PO₄³⁺] = 2S
(потому что при растворении 1 моль фосфата кальция получается 2 моль фосфат-ионов)
Ks (Ca₃(PO₄)₂) = [Ca²⁺]³ * [PO₄³⁺]² = (3S)³ * (2S)² = 27*4*S⁵ = 108*S⁵=
= 2,0*10⁻²⁹
S=⁵√(2,0*10⁻²⁹/108) = 7.1*10⁻⁷ моль/л
Ag₃PO₄ ⇄3 Ag⁺ + PO₄³⁻
Ks (Ag₃PO₄) = [Ag⁺]³ * [PO₄³⁻] = 1,3*10⁻²⁰
S=[Ag⁺] / 3 = [PO₄³⁻]
[Ag⁺] = 3S
[PO₄³⁻] = S
Ks (Ag₃PO₄) = [Ag⁺]³ * [PO₄³⁻] = (3S)³ * S = 27*S⁴ = 1,3*10⁻²⁰
S = ⁴√(1,3*10⁻²⁰ / 27) = 4.7*10⁻⁶ моль/л
Растворимость фосфата кальция ниже, чем растворимость фосфата серебра. Реакция идет не в прямом, а в обратном направлении. . Фосфат серебра не образуется. Решения нет.