1. А) N2 + 3Н2 = 2NН3 - соединения
Б) 3Mg + 2H3РО4 = Mg3(РО4)2 +3 H2↑ - замещения
В) 2Al(OH)3 = Al2O3 + 3H2O - разложения
Г) 2Cu2O = 4Cu + O2↑ - разложения
2. Na2CO3 + 2HCl = 2NaCl + H2O + CO2 - ионного обмена.
признаки: выделение воды и газа, индикатор показывает нейтральный pH (в первом растворе (Na2CO3) изначально показывалась щелочная среда, во втором (HCl) - кислая)
2 + + 2+2=2+2+ H2O + CO2
+ 2=H2O + CO2
3. 2Mg+O2=2MgO
Магний+кислород=оксид магния
MgO+2HCl=MgCl2+H2O
оксид магния+соляная кислота=хлорид магния +вода
MgCl2+2KOH=Mg(OH)2+2KCl
хлорид магния+гидроксид калия= гидроксид магния + хлорид калия
4. 2 + 6 =2 +3
--3e-> 3 2 окислитель
2-+2e-> 2 3 восстановитель
Объяснение:
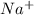

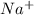
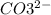

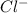


Например:
взаимодействие сильной кислоты и сильного основания.
NaOH + HCl = NaCl + H2O
взаимодействие слабой кислоты и сильного основания
СH3COOH + KOH = CH3COOK + H2O
взаимодействие слабого основания и сильной кислоты
HNO3 + NH4OH = NH4NO3 + H2O
взаимодействие слабой кислоты и слабого кислоты
H2CO3 + NH4OH = (NH4)2CO3 + H2O
Так же реакции нейтрализации бывают чаще всего экзотермическими(идут с выделением тепла, т.к. распространённо добавление в пробирки сильных кислот к сильным щелочам), необратимыми и обратимыми(опять же, если оба вещества сильные).
2. Благодаря полной нейтрализации веществ происходит реакция ионного обмена, полноту которой можно узнать при индикаторов. А так же этот метод применяют в микробиологии,
используемый для в лаборатории для диагностики серологическом тесте, в котором антитела имунной сыворотки тормозят активность микроорганизмов, а так же токсинов, выделяемых ими.
3. Водород можно получить взаимодействием цинка с хлорной кислотой:
2Zn + 2HCl = 2ZnCl + H2 (стрелочка вверх).
Есть вариант через аппарат Киппа и электролиз воды.
Допустим, тебе пришлось проделать какой-либо из этих опытов. Мы получали водород электролизом воды. Этот опыт хорош тем, что чистота водорода близка к 100 процентам и он достаточно прост. Пропускаем электрический ток. Наши пробирки расположены на катоде и аноде.На катоде будет вдород (кстати, это легко понять - меленьких пузырьков будет больше, чем у кислорода), а на аноде - кислород, как побочный продукт. Прекращаем пропускание электрического тока. Очень аккуратно достаём пробирку, зажимая её при этом указательным пальцем, чтобы большая часть водорода не улетучилась и не провзаимодействовала с кислородом. Или достать при газоотводной трубки и пробки.
Далее, чтобы проверить, есть ли в нашей пробирке чистый водород ,необходима горелка. Она должна быть зажжённой( может пригодиться и лучинка). Надо поднести пробирку зажжённой горелке(лучинке)и убрать палец с горлышка(или вынуть пробку). Если водород чистый, то прозвучит хлопок(такой характерно громкий чпок). Если наш водород по какой-то причине провзаимодействовал с кислородом, то в место хлопка будет свист.
Проверка на чистоту необходима для того, чтобы не было смеси кислорода с водородом. Если её(проверки) не будет, то при лабораторном опыте может произойти взрыв и пробирка расколется. Это прежде всего опасно для жизни, ибо осколки могут повредить тело, а если в пробирке была кислота, то приведёт к серьёзным ожогам.