Хе, габриелян:DD
Состав - H2SO4 - думаю пояснять не надо
Тип и класс - сложное вещество - кислоты
Тип связи - ковалентная полярная
Физ. св - ва - тяжёлая маслянистая жидкость без цвета и запах, с кислым «медным» вкусом.
Хим. св - ва -
- вступпает в реакцию со щелочами(при этом нейтрализуясь):
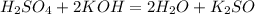
- вступает в реакцию с оксидами металлов - т.е. с основными оксидами:
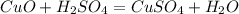
- реагирует с металлами, кроме золота и платины, примеры реакций:
- металлы до водорода:
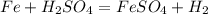
- с металлами после водорода реагирует только лишь концентрированная(помним, что с золотом и платиной реакция не идет):
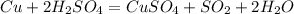
В лаборатории азотную кислоту получают действием концентрированной серной кислотой на нитраты:
NaNO3+H2SO4=NaHSO4+HNO3
Физические свойства:
Азотная кислота- бесцветная летучаю жыдкость, плотность 1,52 г/мл, с едким запохом, которая при температуре -42 по Цельсию переходит в кристаллическое состояние, гигроскопична.
Химические свойства:
Азотная кислота относится к числу наиболее сильных кислот. Степень диссоциации 0,1 М раствора её равна 82%. В водных растворах полностью диссоциирует на ионы Н+ и NO3-:
HNO3знак диссоциацииH+NO3
Является сильным окислителем и в разбавленных растворах.
Несколько примеров окислительно-восстановительныз реакций с участием азотной кислоты:
Ag+2HNO3(конц.)=AgNO3+NO2стрелка вверх+H2O
3Ag+4HNO3(разб.)=3AgNO3+NOстрелка вверх+2H2O
Азотная кислота не реагирует с Pt, Rh, Ir, Pb, Au.
Может частично окислять соляную кислоту:
2HNO3+6HClзнак диссоциации3Cl2+2NO+4H2O
HNO3+3HClзнак диссоциации3Cl+NO+H2O
C2H4+HCL-->C2H5CL
C2H5CL-->C2H4+HCL
C2H4+h2O-->C2h5OH
C2H5OH-->C2H4+H2O
C2H4+Br2-->C2H4Br2
C2H4Br2-->C2H4+Br2
C2H4+H2-->C2H6
C2H6+CL2-->C2H5CL+HCL
2C2H5CL+2Na-->C4H10+2NaCL
C4H10--> CH2=CH-CH2-CH3+H2
CH2=CH-CH2-CH3 -->CH2=CH-CH=CH2
nСH2=CH-CH=CH2 -->( - CH2-CH=CH-CH2-)n