6 г х моль
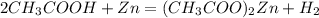
120 г 1 моль
1. Знайдемо чисту массу етанової кислоти у розчині:
m(CH3COOH)=m(розчину)*w(CH3COOH)=50*0,12=6 г
2. Підставивши цю масу у рівняння,розрахуємо кількість речовини водню:
при взаємодії 120 г кислоти виділяється 1 моль водню, а
при -- // -- 6 г____________________х г, звідки
х=6*1/120=0,05 моль
3. А тепер з формули по визначенню кількості речовини, знайдемо:
а) m(H2)=M(H2)*v(H2)=2*0,05=0,1 г
б) V(H2)=Vm(H2)*v(H2)=22,4*0,05=1,12 л
m(C₂H₅OK) = w * m(раствора) = 0.04 * 240 = 9.6 г
Пишем реакцию
2C₂H₅OH + 2K = 2C₂H₅OK + H₂
Пусть на реакцию тратится х моль этанола, значит также идет х моль калия, образуется х моль этилата калия и уходит из раствора х/2 моль водорода
Рассуждаем теперь так:
- в начальный раствор добавили 39х г калия (значит и масса конечного раствора увеличилась на столько же)
- образовалось в ходе реакции 84х г этилата калия
- из раствора улетело х г водорода (значит масса конечного раствора уменьшилась на столько же)
Сгруппируем это все и сделаем пересчет на 8%-ный раствор
Зная количество вещества калия можем посчитать его массу
m(K) = n * M = 0.118577 * 39 = 4.6245 г