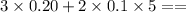
a)3CaCl₂ + 2Na₃PO₄ = 6NaCl + Ca₃(PO₄)₂
3Ca(2+) + 6Cl(-) + 6Na(+) + 2PO₄(3-) = 6Na(+) + 6Cl(+) + Ca₃(PO₄)₂
3Ca(2+) + 2PO₄(3-) = Ca₃(PO₄)₂
Ca₃(PO₄)₂ выпадает в осадок, поэтому на ионы не расладывается
б)H₂SO₄ + Ba(NO₃)₂ = 2HNO₃ + BaSO₄
2H(+) + SO₄(2-) + Ba(2+) + 2NO₃ = 2H(+) + 2NO₃(-) + BaSO₄
Ba(2+) + SO₄(2-) = BaSO₄
BaSO₄ выпадает в осадок, поэтому на ионы не расладывается
в)BaCl₂ + K₂CO₃ = 2KCl + BaCO₃
Ba(2+) + 2Cl(+) + 2K(+) + CO₃(2-) = 2K(+) + 2Cl(-) + BaCO₃
Ba(2+) + CO₃(2-) = BaCO₃
BaCO₃ выпадает в осадок, поэтому на ионы не расладывается
Коррозионные процессы отличаются широким распространением и разнообразием условий и сред, в которых они протекают. Поэтому пока нет единой и всеобъемлющей классификации встречающихся случаев коррозии.
По типу агрессивных сред, в которых протекает процесс разрушения, коррозия может быть следующих видов:
газовая коррозия; атмосферная коррозия; коррозия в неэлектролитах; коррозия в электролитах; подземная коррозия; биокоррозия; коррозия под воздействием блуждающих токов.
По условиям протекания коррозионного процесса различаются следующие виды:
контактная коррозия; щелевая коррозия; коррозия при неполном погружении; коррозия при полном погружении; коррозия при переменном погружении; коррозия при трении; межкристаллитная коррозия; коррозия под напряжением.
По характеру разрушения:
сплошная коррозия, охватывающая всю поверхность: равномерная; неравномерная; избирательная[1]; локальная (местная) коррозия, охватывающая отдельные участки: пятнами; язвенная; точечная (или питтинг); сквозная; межкристаллитная (расслаивающая в деформированных заготовках и ножевая в сварных соединениях).
Главная классификация производится по механизму протекания процесса. Различают два вида:
химическую коррозию; электрохимическую коррозию. Корро́зия (от лат. corrosio — разъедание) — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. В общем случае это разрушение любого материала, будь то металл или керамика, дерево илиполимер. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Пример — кислородная коррозия железа в воде: 4Fe + 6Н2О + ЗО2 = 4Fe(OH)3. Гидратированный гидроксид железа Fe(OН)3 и является тем, что называют ржавчиной.
Объяснение: