24 г 26,7 г, х г у г
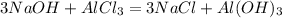
120 г 133,5 г 78 г
1. Сначала определим,какое из исходных веществ прореагирует полностью,т.е. без остатка,приняв,например,массу хлорида алюминия за Х:
для полного взаимодействия 120 г гидроксида натрия необходимо 133,5 г хлорида алюминия, а для --//-- 24 г______________________________х г, откуда
х=24*133,5/120=26,7 г
2. Так как все вещества прореагировали полностью,то массу осадка можно рассчитать по массе любого из исходных веществ:
при взаимодействии 120 г гидроксида натрия образуется 78 г осадка, а
при -- // -- // -- 24 г____________________________у г, откуда
у=24*78/120=15,6 г
Найти: m(KNO3)-?
Решение: уравнение реакции
KOH+HNO3=KNO3+H2O
Для определения цвета лакмуса нужно определить, какое вещество взяли в избытке. Масса гидроксида калия в растворе составляет 5*100/100=5 грамм. Масса азотной кислоты в растворе составляет 10*150/100=15 грамм.
N(KOH)=5/56=0,1 моль, N(HNO3)=15/63=0,24 моль.
Кислота взята в избытке, поэтому останется после реакции и при добавлении лакмуса раствор окрасится в красный цвет.
При взаимодействии 56 грамм КОН образуется 101 грамм нитрата калия, а из 5 грамм образуется Х.
Х=5*101/56=9 грамм.
ответ: m(KNO3)=9 грамм, лакмус будет красный.