Дано:
V(H₂)=11,2л.
Vm=22,4л./моль
m(Fe)-?
1. Определим количество водорода в 11,2л.:
n₁(H₂)=V(H₂)÷Vm
n₁(H₂)=11,2л.÷22,4л./моль=0,5моль
2. Запишем уравнение реакции:
Fe₂O₃+3H₂=2Fe+3H₂O
по уравнению реакции:
n(H₂)=3моль n(Fe)=2моль
по условию задачи:
n₁(H₂)=0,5моль n₁(Fe)=0,33моль
3. Определим молярную массу железа:
M(Fe)=56г./моль
4. Определим массу железа количеством вещества 0,33моль:
m(Fe)=n₁(Fe)xM(Fe)
m(Fe)=0,33мольx56г./моль=18,48г.
5. ответ: при взаимодействии 11.2 литра водорода с оксидом железа (III) образуется 18,48г. железа.
200 л 250 л х л
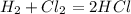
1 объем 1 объем 2 объем
1. Согласно уравнения и закона объемных отношений газообразных веществ,видим,что на 1 объем(1 л или 1 м в кубе) водорода необходимо 1 объем хлора,значит для полного взаимодействия 200 л водорода пойдет 200 л хлора.Т.е. в остатке останется хлор объемом:250-200 = 50 л.
2. Найдем объем хлороводорода,который образуется в результате реакции:
при взаимодействии 1 объема водорода образуется 2 объема хлороводорода, а
при -- // -- 200 л_______________________х л, откуда
х=200*2/1=400 л
m(соли)=w*m(раствора)=0.15*200=
30г
m(воды)=200-30=170г