Привет! Сейчас все запишем:
Дано: w₁(H₂SO₄) = 63% , w₂(H₂SO₄)=20%
II. Запишем формулы // Проведем вычисления:
w(E)=m(E)/m(раствора) · 100%
m(E)=w(E)*m(раствора) / 100%
// Пусть мы взяли 100 грамм этого вещества:
m₁(H₂SO₄)=63*100 / 100 = 63 грамма
Теперь сделаем соотношение между массой серной кислоты и новой массой вещества (2):
63 грамма - 20 %
х грамм - 100%
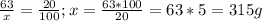
III. Отнимаем от 315 наши 63 грамма кислоты
315 - 63 = 252 грамма воды, при этом в первом растворе было 37 грамм воды (100-63 = 37)
Найдем нужную нам массу воды, которую нужно добавить до 63%-ной серной кислоте, чтобы получить 20%-ный раствор:
252 - 37 = 215 грамм
Готово! Есть вопросы? Напишите, с радостью отвечу на них
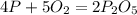
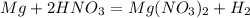 ↑
↑
H2+Cl2=2HCl
Ca+2HCl=CaCl2+H2
Поставте как лучший ответ