
845 г
Объяснение:
Можна виразити олеум у вигляді концентрації сульфатної кислоти, а саме
%кислоти = 100 + 18/80 * %олеуму = 100 + 18/80 * 25 = 105.625%
А потім зробити дану задачу методом "хреста", але підемо зрозумілішим, хоча і довшим шляхом
Рахуємо масу оксиду в олеумі
m(SO₃) = m(олеуму) * w = 320 * 0.25 = 80 г
Напишемо рівняння, щоб були ясніші подальші дії
SO₃ + H₂O = H₂SO₄
80 г оксиду, це якраз його 1 моль, а за рівнянням реакції води також потрібно 1 моль, тобто 18 г. Маса 100%-вої сульфатної кислоти буде 320 + 18 = 338 г
Ну і залишилось вияснити, скільки ще треба води, щоб розчин став 40%-вим
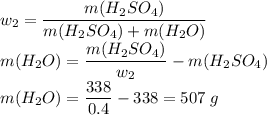
Отже, маса кінцевого розчину
m(олеуму) + m₁(H₂O) + m₂(H₂O) = 320 + 18 + 507 = 845 г