Объяснение:
4 г Х г Х л
3Ca + 2H3PO4 = Ca3(PO4)2 + 3H2
n=3 моль n=1 моль n=3 моль
М = 40 г/моль М=310 г/моль Vm=22,4 л/моль
m=120 г m=310 г V = 67,2 л
4 г Са - Х г Са3(РО4)2
120 г Са - 310 г Са3(РО4)2
m(Ca3(PO4)2) = 4 * 310 / 120 = 10,33 г
4 г Са - Х л Н2
120 г Са - 67,2 л Н2
V(H2) = 4 * 67,2 / 120 = 2,24 л
Принцип Ле-Шателье:
Если на систему, находящуюся в равновесии, производится внешнее воздействие (изменяются концентрация, температура, давление), то равновесие смещается в сторону той реакции, которая ослабляет это воздействие.
1. Концентрация:
а) при увеличении концентрации исходных веществ равновесие смещается в сторону прямой реакции (вправо);
б) при увеличении концентрации продуктов реакции равновесие смещается в сторону обратной реакции (влево).
2. Температура: При увеличении температуры равновесие всегда смещается в сторону эндотермической реакции.
3. Давление: При увеличении давления равновесие смещается в сторону той реакции, которая приводит к уменьшению объёмов газообразных веществ.
Реакция:
Пусть в исходной смеси было х грамм KCl, тогда масса KBr равна: m(KBr)=1,60-х
M(KBr)=119г/моль.
Тогда в ходе реакции было использовано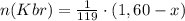 молей KBr и образовалось столько же молей KCl.
молей KBr и образовалось столько же молей KCl.
M(KCl)=74,5 г/моль.
Выразим массу полученного KCl: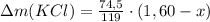
Добавим х грамм, которые были в начале, получим:
Получаем уравнение: 0,63 * (1,60 - x) +x =1,36
0,37x = 0,35
Решив уравнение получаем х=0,95 грамм.
Тогда массовая доля KCl в исходной смеси равна отношению масс KCl к массе смеси: 0,95/1,60=0,59=59%.