1) ковалентная-неполярная связь между двумя сходными неметаллами:
ответ: 4
2) ковалентная-полярная связь между двумя разными неметаллами:
ответ: 2
3) наибольшая электроотрицательность у неметаллов:
ответ: 4
4) 1 --б 2 --- в 3---4
5) схема в фото. тип связи: ковалентно-неполярная
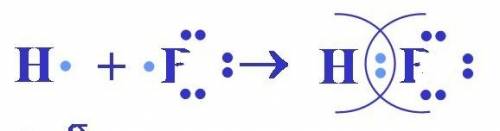
6) схема в фото. тип связи: ковалентно-полярная
2в комментарии как у 1 варианта
1) ответ: 3
2) ответ: 1
3) ответ: 3
4) 1 --- б 2-- в 4--а
1) схема в фото. тип связи: ковалентно-неполярная
2) схема в фото. тип связи: ковалентно-полярная
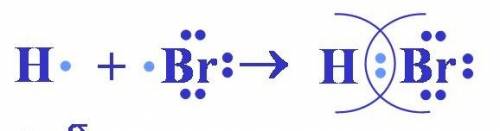
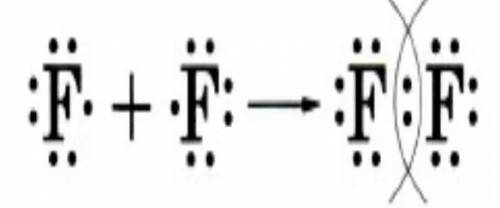
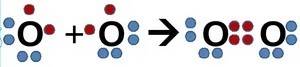
1) Определим массу 1 моля безводного Na₂SO₃ и кристаллогидрата Na₂SO₃*10Н₂О:
М(Na₂SO₃) = 2*23 + 32 + 3*16 = 126 г/моль
М(Na₂SO₃*10Н₂О) = 126 + 10*18 = 306 г/моль
2) Тогда массовая доля безводного Na₂SO₃ в его кристаллогидрате составляет:
ω = 126/306 = 0,4118
3) Если концентрация раствора выражена в долях единицы, то массу растворенного вещества в граммах находят по формуле:
m(в-во) = ω * m(p-p)
где: m(p-p) - масса раствора в граммах, ω - массовая доля растворенного вещества, выраженная в долях единицы.
4) Обозначим массу кристаллогидрата через Х, а так как масса растворенного вещества не изменяется, то можем составить уравнение:
0,4118*Х = 0,1 * (Х + 800)
0,3118Х = 80
Х = 256,57
ответ: 256,57 г
Дано:
m(P)=310г.
m(P₂O₅)-?
1. Определим количество вещества в 310г. фосфора:
n(P)=310г.÷31г./моль=10моль
2. Запишем уравнение реакции:
4P+5O₂=2P₂O₅.
3.Анализируем уравнение реакции: по уравнению реакции из 4моль фосфора образуется 2 моль оксида фосфора(V) . По условию задачи 10моль фосфора, значит образуется 5моль оксида фосфора(V)
4. Определим молярную массу оксида фосфора(V) и его массу количеством вещества 5моль:
M(P₂O₅)=31x2+16x5=142г./моль
m(P₂O₅)=n(P₂O₅)xM(P₂O₅)=5мольx142г./моль=710г.
5.ответ: при горении 310г. фосфора образуется оксида фосфора(V) массой 710г.