С₈Н₁₈
Объяснение:
При крекинге алканов образуются новые алканы и алкены
Если есть плотность одного из продуктов, то можем (при условии что это газ) посчитать его молярную массу
M(газа) = ρ · Vm = 2.589 · 22.4 = 58 г/моль
Пусть формула образовавшегося вещества 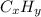 . Напишем следующее соотношение
. Напишем следующее соотношение
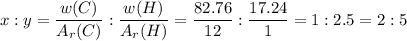
Простейшая формула соединения - C₂H₅ с молярной массой 29 г/моль, а реальная молярная масса 58 г/моль, поэтому истинная формула соединения - С₄Н₁₀ - бутан. Значит второй углеводород был бутен. Исходное вещество было алканом и имело 8 атомов углерода. Это был октан - С₈Н₁₈
Пишем реакцию крекинга
С₈Н₁₈ = С₄Н₁₀ + С₄Н₈
Пишем реакцию синтеза октана по Фишеру-Тропшу
8CO + 17H₂ = С₈Н₁₈ + 8H₂O
С₈Н₁₈
Объяснение:
При крекинге алканов образуются новые алканы и алкены
Если есть плотность одного из продуктов, то можем (при условии что это газ) посчитать его молярную массу
M(газа) = ρ · Vm = 2.589 · 22.4 = 58 г/моль
Пусть формула образовавшегося вещества 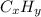 . Напишем следующее соотношение
. Напишем следующее соотношение
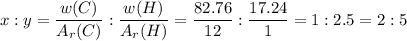
Простейшая формула соединения - C₂H₅ с молярной массой 29 г/моль, а реальная молярная масса 58 г/моль, поэтому истинная формула соединения - С₄Н₁₀ - бутан. Значит второй углеводород был бутен. Исходное вещество было алканом и имело 8 атомов углерода. Это был октан - С₈Н₁₈
Пишем реакцию крекинга
С₈Н₁₈ = С₄Н₁₀ + С₄Н₈
Пишем реакцию синтеза октана по Фишеру-Тропшу
8CO + 17H₂ = С₈Н₁₈ + 8H₂O
1) Так как вода имеет плотность 1 г/л, то 2 литра воды или 2000 мл имеют массу 2000 г.
2) Бромоводород - это газ, для любого газа верно утверждение, что 1 моль газа занимает объём 22,4 л. Масса 1 моля HBr равна: МHBr) = 1,008 + 79,94 = 80,91 г/моль.
80,91 г HBr занимают объем 22,4 л
Х г HBr 5 л
Х = 80,91*5/22,4 = 18,06 г
3) 18,06 г бромоводорода растворили в 2000 г воды, получили раствор массой (18,06 + 2000) = 2018,06 г
Массовая доля растворенного вещества (выраженная в долях единицы) находят по формуле:
ω = m(в-во) / m(р-р) = 18,06/2018,06 = 0,00895 (или 0,895%)
ответ: 0,895%