№1. Дано:
m(Mg)=48 г
______________________
m(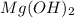 )=?
)=?
2 моль x
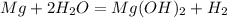
1 моль 1 моль
n(Mg)=m/M=48г/24г/моль=2 моль
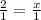 х=n(
х=n(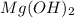 )=2 моль
)=2 моль
m(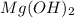 )=n*M=2 моль* 42г/моль=84 г
)=n*M=2 моль* 42г/моль=84 г
ответ: 84 г
С твоим ответом не сошлось, т.к. у тебя реакция неправильная.
№2. а, в, г, ж
№3. Дано:
m(HCl)=73 г
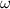 (HCl)=4,5%
(HCl)=4,5%
__________________________
m(NaCl)=?
0,09 моль х
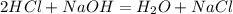
2 моль 1 моль
m(HCl)=73г*4,5%/100%=3,285 г
n(HCl)=3,285г/36,5г/моль=0,09 моль
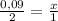
x=n(NaCl)=0,045 моль
m(NaCl)=0.045 моль*58,5г/моль=2,6325 г
ответ: 2,6325 г
Дано:
m(технического CaCO₃)=800г.
ω%(примесей в CaCO₃ )=12,%
Vm=22,4л./моль
V(CO₂)-?
1. Определим массу чистого карбоната кальция:
m(CaCO₃)=m(технического CaCO₃)xω%(примесей в CaCO₃ )÷100%
m(CaCO₃)=800г.×12,%÷100%=96г.
2. Определим молярную массу карбоната кальция и его количество вещества в 96г:
M(CaCO₃)=100г./моль
n₁(CaCO₃)=96г÷100г./моль=0,96моль
3. Запишем уравнение реакции разложения карбоната кальция:
CaCO₃ = CaO + CO₂
по уравнению реакции:
n(CaCO₃)=n(CO₂)=1моль
по условию задачи:
n₁(CaCO₃)=n₁(CO₂)=0,96моль
4. Определим объем оксида углерода(IV) :
n₁(CO₂)=0,96моль
V(CO₂)=n₁(CO₂)x22,4л./моль
V(CO₂)=0,96мольх22,4л./моль=21,5л.
5. ответ: при разложении 800г. технического карбоната кальция с массовой долей примесей 12% образовалось 21,5л. углекислого газа (оксида углерода(IV).
по кислотному остатку. НАпример соль NaCl Натрий тут металл, а хлор - кислотный остаток. Соль - хлорид.
SO4 -сульфат
SO3-сульфит
S-Сульфид
CO3-карбонат
NO3-нитрат
NO2-нитрит
SiO3-силикат
Остальные имеют названия по элементу (Фтор - фторид и т. п.)