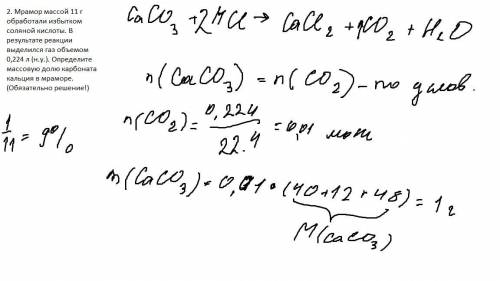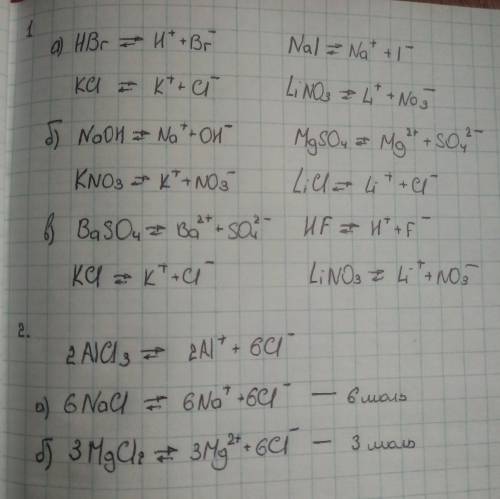
Відповідь:
Пояснення:
0 0 +2 -2
2Сu + O2 = 2CuO соединения реакция
Cu - 2e = Cu +2 восстановитель
O2 + 4e = 2O-2 окислитель
+2 0 0 +1
CuO + H2= Cu +H2O замещения реакция
Cu + 2e = Cu окислитель
H2 - 2e - 2H - восстановитель
0 0 +3 -2
4Fe + 3O2 = 2 Fe2O3 соединения реакция
Fe -3 e = Fe+3 восстановитель
O2 + 4e = 2O-2 окислитель
+3 -2 0 0 +1
Fe2O3 +3H2 =2 Fe + 3H2O замещения
Fe + 3e = Fe окислитель
H2 - 2e =2H восстановитель
Fe + H2SO4 = FeSO4 + H2
Zn + 2HCl = ZnCl2 + H2
Задача Zn + 2HCl = ZnCl2 + H2
73г/моль 2 г/моль за реакцией
х г 2,24 г за задачей
х =73 г/моль * 2,24 г / 2 г/моль = 81,76г
Объяснение:
1
а) NH4Cr2O7 - N- (-3) H - (+1) Cr (+6) O(-2)
б) K2MnO4 Mn - (+7) K (+1) O - (-2)
c) Ca (+2) O (-2) H(+1)
d) H(+1) S(+4) O(-2)
2) Внизу файл прикреплен
3) Кальций , барий - Имеют электронную конфигурацию ns2, образуют оксиды состава RO
Калий, натрий - Все они имеют один s-электрон на наружном электронном слое
Алюминий бор - На внешнем энергетическом уровне находится 3 электрона (2 s и 1 p)
4) А) 1) В судостроение засчет своей легкости
2) В электронике за счет хорошей проводимости электрического тока
Б) Их хранят под слоем керосина, потому что они очень энергично окисляются при контакте с воздухом, образуя оксиды и пероксиды
В) Радиус атома рубидия больше чем у натрия, значит электрон удален от ядра дальше чем у натрия, а следовательно и забрать его легче