6 г х моль
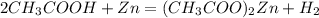
120 г 1 моль
1. Знайдемо чисту массу етанової кислоти у розчині:
m(CH3COOH)=m(розчину)*w(CH3COOH)=50*0,12=6 г
2. Підставивши цю масу у рівняння,розрахуємо кількість речовини водню:
при взаємодії 120 г кислоти виділяється 1 моль водню, а
при -- // -- 6 г____________________х г, звідки
х=6*1/120=0,05 моль
3. А тепер з формули по визначенню кількості речовини, знайдемо:
а) m(H2)=M(H2)*v(H2)=2*0,05=0,1 г
б) V(H2)=Vm(H2)*v(H2)=22,4*0,05=1,12 л
2NaOH+CO2-->Na2CO3+H2O
2Na⁺+2OH⁻+CO2-->2Na⁺+CO²⁻₃+H2O
2OH⁻+CO2-->CO²⁻₃+H2O
NaOH+HCL-->NaCL+H2O
Na⁺+OH⁻+H⁺+CL⁻-->Na⁺+CL⁻+H2O
OH⁻+H⁺-->H2O
2NaOH+CuSO4-->Na2SO4+Cu(OH)2↓
2Na⁺+2OH⁻+Cu²⁺+SO²⁻₄-->2Na⁺+SO²⁻₄+Cu(OH)2↓
2OH⁺+Cu²⁺-->Cu(OH)2↓