Реакция синтеза оксида фосфора описывается следующим уравнением химической реакции:
4Р + 5О2 = 2Р2О5;
4 атома фосфора вступают во взаимодействие с 5 молекулами кислорода. При этом синтезируется 2 молекулы оксида фосфора.
Вычислим химическое количество вещества, находящееся в фосфоре массой 5 грамм.
М Р = 31 грамм/моль;
N Р = 5 / 31 = 0,161 моль;
Из такого количества фосфора возможно синтезировать 0,161 / 2 = 0,081 моль его оксида.
Вычислим его вес.
Для этого умножим количество вещества на его молярный вес.
М Р2О5 = 31 х 2 + 16 х 5 = 142 грамм/моль;
м Р2О5 = 142 х 0,081 = 11,502 грамм;
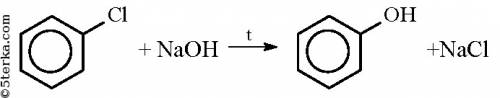
При действии на хлорбензол щелочи при высокой температуре происходит замещение атома хлора на гидроксильную группу и получается фенол.
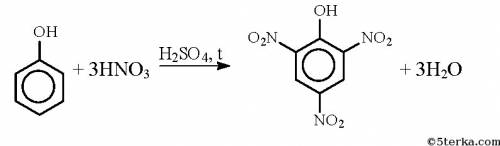
При реакции фенола со смесью азотной и серной кислот образуется пикриновая кислота (2,4,6-тринитрофенол).
Значит, процесс проводится в несколько стадий :
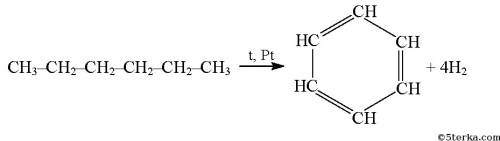
1. Хлорирование бензола до монохлорбензола:
C6H6 + Cl2 = C6H5Cl + HCl
2. Нитрования монохлорбензола до динитрохлорбензола смесью серной и азотной кислот:
C6H5Cl + 2HNO3 = C6H3(NO2)2Cl +2H2O
3. Обработка динитрохлорбензола каустической содой (гидроокисью натрия) с получением динитрофенолята натрия:
C6H3(NO2)2Cl + 2NaOH = C6H3(NO2)2ONa + NaCl + H2O
4. Омыление динитрофенолята натрия серной кислотой с получением динитрофенола:
2 C6H3(NO2)2ONa + H2SO4 = 2 C6H3(NO2)2OH + Na2SO4
5. Получение тринитрофенола (пикриновая кислота) обработкой смесью серной и азотной кислот:
C6H3(NO2)2OH + HNO3 = C6H3(NO2)3OH + H2O
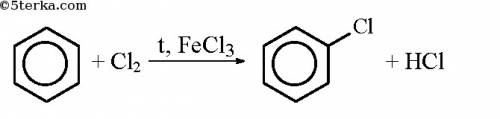
2Al + 3S = Al2S3
n(Al) = 26г : 27г/моль = 0.963моль
n(S) = 54г : 32г/моль = 1.6875моль(Избыток)
n(Al) : n(Al2S3) = 2 : 1
m(Al2S3) = 0.48моль × 150г/моль = 72г