1. Кремний с серной кислотой не реагирует. Алюминий же в ней растворяется с выделением водорода:
2 Al + 3 H2SO4 = Al2(SO4)3 + 3 H2 ↑
2 моль 3 моль
х моль 0,6 моль
Количество вещества водорода равно 13,44 л/ 22,4 л/моль = 0,6 моль.
Количество вещества алюминия по уравнению реакции равно:
х = 2*0,6/3 = 0,4 моль
2. Кремний и алюминий растворяются в щелочах с выделением водорода
2Al + 2NaOH + 6H2O = 2 K[Al(OH)4] + 3H2 ↑
Si + 2NaOH + H2O = Na2SiO3 + H2 ↑
Количество вещества водорода равно 17,92 л/ 22,4 л/моль = 0,8 моль.
Из них 0,6 моль выделилось за счет реакции с алюминием (поскольку для второго опыта был взят образец той же смеси алюминия и кремния такой же массы). Значит, за счет реакции кремния с щелочью выделилось 0,2 моль водорода.
Si + 2NaOH + H2O = Na2SiO3 + H2 ↑
1 моль 1 моль
у моль 0,2 моль
Количество вещества кремния согласно уравнению реакции также равно 0,2 моль.
Состав смеси: 0,2 моль Si, 0,4 моль Al
Для определения массовой перейдем от количества вещества к массе вещества
m(Si) = n(Si)*M(Si) = 0,2 моль * 28,1 г/моль = 5,62 г.
m(Al) = n(Al)*M(Al) = 0,4 моль * 27,0 г/моль = 10,8 г.
Масса образцов m = m(Si) + m(Al) = 5.62 + 10.8 = 16.42 г.
Массовая доля кремния w(Si) = m(Si) / m = 5.62 г / 16.42 г = 0,342 = 34,2%
Получено 19,6 г сульфата хрома (III) Cr₂(SO₄)₃ и 3,36 л водорода
Объяснение:
Дано: m(Cr) = 5,2 г; m(H₂SO₄) = 98 г.
Найти: m(Cr₂(SO₄)₃); V(H₂).
Решение.
2Cr + 3H₂SO₄ → Cr₂(SO₄)₃ + 3H₂
По уравнению реакции хром и серная кислота реагируют в отношении 2 моль : 3 моль. Найдем количество вещества в заданных массах:
Молярная масса M(Cr) = 52 г/моль
Количество вещества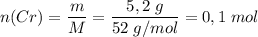 .
.
M(H₂SO₄) = 2 + 32 + 64 = 98 г/моль
На 0,1 моль Cr требуется 0,15 моль H₂SO₄. Серная кислота дана в избытке. Расчет ведем по хрому.
По уравнению реакции
n(Cr) : n(Cr₂(SO₄)₃) : n(H₂) = 2 : 1 : 3 = 0,1 моль : 0,05 моль : 0,15 моль
Найдем массу образовавшегося сульфата хрома (III) Cr₂(SO₄)₃
M(Cr₂(SO₄)₃) = 2*52 + 32*3 + 16*4*3 = 104 + 96 + 192 = 392 г/моль
m(Cr₂(SO₄)₃) = n*M = 0,05 моль * 392 г/моль = 19,6 г.
Найдем объем выделившегося водорода:
V(H₂) = n*Va = 0,15 моль * 22,4 л/моль = 3,36 л.