mр-ра = 400г
ω = 10% = 0.1
+ m = 50г
ω₂ - ?
mв-ва₁ = mр-ра × ω = 400г × 0.1 = 40г
mв-ва₂ = 40г + 50г = 90г
mр-ра₂ = 400г + 50г = 450г
ω₂ = mв-ва ÷ mр-ра × 100% = 90г ÷ 450г × 100% = 20%
1)2KNO3+CaCl2 → Ca(NO3)2+2KCl. Данная реакция не пойдёт(не получится) в ионном виде так как все вещества растворимы, а надо хотя чтоб одно было нерастворимым
2) K2SO4+2NaOH → 2KOH+Na2SO4. Данная реакция не пойдёт(не получится) в ионном виде так как все вещества растворимы, а надо хотя чтоб одно было нерастворимым
3) CuSO4+2NaOH → Cu(OH)2↓+Na2SO4
Cu(2+)+SO4(2-)+2Na(+)+2OH(-) → Cu(OH)2↓+2Na(+)+SO4(2-)
Cu(2+)+2OH(-) → Cu(OH)2↓
4) 2HCl+Mg(NO3)2 → MgCl2+2HNO3. Данная реакция не пойдёт(не получится) в ионном виде так как все вещества растворимы, а надо хотя чтоб одно было нерастворимым
Нашлось, по крайней мере два соединения, гидрида, в которых массовая доля водорода равна 12,5%:
гидрид лития LiH и гидрид кремния (силан) SiH₄.
Объяснение:
Массовая доля водорода в соединении с другим элементом составляет 12,5% или 0,125.
Тогда массовая доля неизвестного элемента в данном соединении равна 100% - 12,5% = 87,5% или 0,875.
Имеется некоторое соединение, гидрид элемента E состава EHₙ , где n - валентность неизвестного элемента E.
Массовая доля водорода и массовая доля элемента E в веществе:
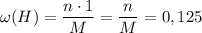 , где M - молярная масса вещества.
, где M - молярная масса вещества.
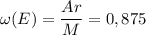
Найдем отношение массовых долей элементов:

Тогда относительная атомная масса элемента E равна Ar = 7n.
1) При n = 1 , Ar = 7, это литий, его валентность равна 1, гидрид имеет формулу LiH.
Сделаем проверку массовых долей лития и водорода:
M(LiH) = 7 + 1 = 8

Верно.
2) При n = 2, Ar = 14. Это азот, но азот в соединении с водородам проявляет валентность III. NH₃. Не подходит.
3) При n = 3, Ar = 21. Элемента с такой атомной массой нет. Не подходит.
4) При n = 4, Ar = 28. Это кремний, гидрид имеет формулу SiH₄ (силан)
Сделаем проверку массовых долей кремния и водорода:
M(SiH₄) = 28 + 4 = 32
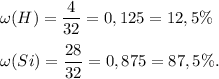
Верно.
1) Если концентрацию раствора выразить в долях единицы, то массу растворенного вещества в граммах находят по формуле:
m(в-во) = ω * m(p-p)
где: m(p-p) - масса раствора в граммах, ω - массовая доля растворенного вещества, выраженная в долях единицы.
То есть, 10% - это 0,1
2) Добавляемая соль - это 100% вещества или 1 в долях единицы.
При добавлении соли масса раствора увеличивается на 50 г. м
Обозначим концентрацию полученного раствора через Х и на основании всего вышеизложенного составляем уравнение:
0,1 * 400 + 1 * 50 = Х * (400 + 50)
40 + 50 = 450Х
Х = 90/450 = 0,2 (или 20%)
ответ: 20%