Объяснение:
а) Формула - Na₂CO₃. Класс - соль.
б, в) Химические свойства:
1. Взаимодействие с кислотами:
Na₂CO₃ + 2HCl → 2NaCl + CO₂ + H₂O (реакция обмена)
2Na⁺ + CO₃²⁻ + 2H⁺ + 2Cl⁻ → 2Na⁺ + 2Cl⁻ + CO₂ + H₂O
CO₃²⁻ + 2H⁺ → CO₂ + H₂O
2. Гидролиз - взаимодействие с водой (реакция обмена)
Na₂CO₃ + H₂O → NaHCO₃ + NaOH (первая ступень)
2Na⁺ + CO₃²⁻ + H₂O → Na⁺ + HCO₃⁻ + Na⁺ + OH⁻
CO₃²⁻ + H₂O → HCO₃⁻ + OH⁻
NaHCO₃ + H₂O → NaOH + H₂CO₃ (CO₂ + H₂O)
Na⁺ + HCO₃⁻ + H₂O → Na⁺ + OH⁻ + H₂CO₃ (CO₂ + H₂O)
HCO₃⁻ → OH⁻ + H₂CO₃ (CO₂ + H₂O)
3. Взаимодействие с солями (не со всеми, главное, что б реакция
Na₂CO₃ + Ca(NO₃)₂ → 2NaNO₃ + CaCO₃↓ (реакция обмена)
2Na⁺ + CO₃²⁻ + Ca²⁺ + 2NO₃⁻ → 2Na⁺ + 2NO₃⁻ + CaCO₃
CO₃²⁻ + Ca²⁺ → CaCO₃↓
4. Разложение при нагревании:
Na₂CO₃ → Na₂O + CO₂↑ (реакция разложения)
5. Взаимодействие с неметаллами (оксилительно-восстановительные реакции)
3Na₂CO₃ + 3Cl₂ → 5NaCl + NaClO₃ + 3CO₂↑
6Na⁺ + 3CO₃²⁻ + 3Cl₂ → 5Na⁺ + 5Cl⁻ + Na⁺ + ClO₃⁻ + 3CO₂↑
3CO₃²⁻ + 3Cl₂ → 5Cl⁻ + ClO₃⁻ + 3CO₂↑
34,5 г
Объяснение:
Дано:
m(FeCl₃) = 100 г
Найти:
m(Fe) - ?
Реакция: 2Fe + 3Cl₂ → 2FeCl₃
Составим пропорцию, учитывая, что и у железа, и у FeCl₃ стоят одинаковые коэффициенты, значит, их количества вещества равны (и их можно сократить)
x 100 г - это массы, т.к. масса железа неизвестна, она x
Fe → FeCl₃
56 162,5 - это молярные массы, находятся по таблице
Менделеева
Ну и теперь крест-накрест и находим массу железа:
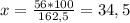 г
г
Cu(0) - 2e-->Cu(+2) |1 (пр.окисление)
N(+5) +1e-->N(+4) |2 (пр.восстан-ие.)
Cu в простом веществе - восстановитель
N(+5) (HNO3) - окислитель
удачи))
Понравилось решение?Жми ЛУЧШИЙ!)