1.
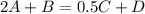
Выражение для константы равновесия:
![K = \frac{[C]^{0.5}[D]}{[A]^{2}[B]}](/tpl/images/0972/8582/67d8a.png)
Очевидно, равновесная концентрация вещества B равна:
![[B] = \frac{0.2^{0.5}*0.1}{38*10^{-2}*0.5^2} = 0.471](/tpl/images/0972/8582/b8eb2.png) моль/дм^3
моль/дм^3
2.
Уравнение, связывающее мольную долю и массовую долю:
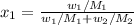
Мольная доля воды в растворе равна:
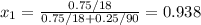
Примем данный раствор идеальным. Тогда равновесное давление паров компонентов над раствором выражается через закон Рауля:
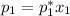
Отсюда находим равновесное давление паров воды над раствором:
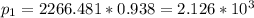 Па
Па
3.
Выражение для степени набухания полимера: (в долях)
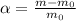
Масса нулевая - масса полимера без воды, масса без индекса - набухший полимер.
Δm = 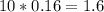 г.
г.
Привет! Сейчас решим
1. Гидроксид натрия реагирует с серной кислотой с образованием сульфата натрия и воды
2NaOH + H2SO4 = Na2SO4 + 2H2O
2) Гидроксид натрия реагирует с серным ангидридом с образованием сульфата натрия
2NaOH + SO3 = Na2SO4 + H2O
3) Гидроксид натрия реагирует с сульфатом меди с образованием сульфата натрия и гидроксида меди
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2
4) Гидроксид натрия под действием температуры разлогается на оксид магния и воду
Mg(OH)2 = MgO + H2O
Готово! Есть вопросы? Напиши и я отвечу