1) Сначала находим массу соли в первом растворе:
m(соли)=m1(раствора)*w1(соли)=280*0,15=42 г
2)Чтобы найти массовою долю,необходимо сначала найти массу второго раствора(после выпаривания):
m2(раствора)=m1(раствора) - m(воды,которую выпарили)=280-120=160 г.Но перед этим необходимо оговориться о том,что так как плотность воды равна 1 г/мл,то объем численно равняется массе.
3)Теперь ничего не стоит найти массовою долю соли в новом(выпаренном растворе),произведя отношение массы соли,так как она при выпаривании не изменяется,к массе нового раствора:
w2(соли)=m(соли)/m2(раствора)=0,26 или 26%
ответ:массовая доля соли в полученном после выпаривания растворе составляет 26%
1) m(KNO3) = 280*0.15=42 г;
2) m(H2O) = 280-42=238 г;
3) m(H2O)ост. = 238-120=118 г;
4) w(KNO3)=42/(42+118)*100% = 26.25%
ответ: массовая доля соли в полученном растворе 26,25%.
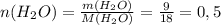 моль
моль
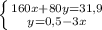
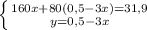
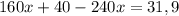
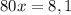
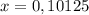 моль (это количество вещества Fe₂O₃)
моль (это количество вещества Fe₂O₃)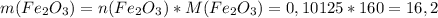 г
г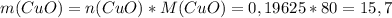 г
г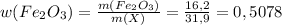 или 50,78% (где m(X) - это масса смеси)
или 50,78% (где m(X) - это масса смеси)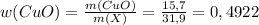 или 49,22%
или 49,22%
1) Находим молярную массу магния:
М(Mg) = 24 г/моль
Тогда 18 г магния составляют:
18/24 = 0,75 моль
2) Уравнения реакции:
2Mg + Si → Mg₂Si
Mg₂Si + 4H₂O → 2Mg(OH)₃ + SiH₄↑
По уравнениям реакций видно, что из 2 молей магния теоретически должно получиться 1 газа (соотношение 2 : 1), значит из 0,75 молей магния должно получиться 0,375 моля газа.
3) Так как 1 моль газа при н.у. занимает объем 22,4 л, то 0,375 молей газа имеют объем:
0,375*22,4 = 8,4 л
4) Тогда выход составляет:
(5,6/8,4)*100% = 66,7%
ответ: 66,7%