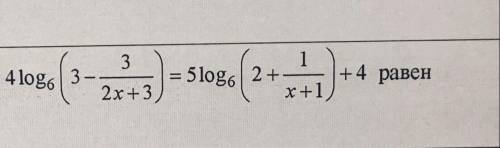
4log₆(3-3/(2x+3))=5log₆(2+1/(x+1))+4 ;
4log₆(6(x+1)/(2x+3))=5log₆( (2x+3)/(x+1) )+4 ;
4㏒₆6+4log₆((x+1)/(2x+3))=5log₆((2x+3)/(x+1))+4 ;
4+4log₆((x+1)/(2x+3))+5log₆ ((x+1)/(2x+3))-4=0; 9log₆(x+1)/(2x+3) =0 ;
log₆ (x+1)/(2x+3) =0; (x+1)/(2x+3) =1; х≠-1.5; x+1=2x+3 ; x= - 2
Существует множество определений философии. Например, философия — дисциплина, изучающая наиболее общие существенные характеристики и фундаментальные принципы реальности и познания, бытия человека, отношения человека и мира. Другой вариант: философия — форма общественного сознания, вырабатывающая систему знаний о фундаментальных принципах бытия и месте человека в мире.Термин "философия" состоит из двух греческих слов "philia" (любовь) и "sophia" (мудрость), т.е. переводится как любовь к мудрости.
Выделяются следующие функции философии:Мировоззренческая. Дает человеку цельное и рациональное мировоззрение ему критически оценивать самого себя и свое окружение.Методологическая. Дает человеку знание и показывает пути, как получать новое знание. Одним из важнейших методов философии является диалектический. Диалектика — это умение осмыслить предмет в его целостности и развитии, в единстве его базовых противоположных свойств и тенденций, в многообразных связях с другими предметами.Прогностическая. Позволяет строить прогнозы о будущем. Есть множество примеров, когда идеи философов значительно опережали свое время. Например, идея древней китайской философии об универсальном характере связей противоположных сил инь и ян нашла свое отражение в знаменитом "принципе дополнительности" Нильса Бора, легшего в основу квантово-механической картины мира.Синтетическая. Данная функция заключается в установлении взаимосвязей между сферами духовного творчества человека.
Пошаговое объ Розчини. Концентрація розчинів
Важливою характеристикою розчинів є їх концентрація – це вміст розчиненої речовини в певному об’ємі (масі) розчину або розчинника. Її виражають наведеними нижче Молярна концентрація (СМ) – це кількість молів розчиненої речовини в 1 л розчину;
Моляльна концентрація компоненту (Сm) – це кількість молів розчиненої речовини в 1 кг (1000 г) розчинника, наприклад, води:
, (7.1)
де m1 і m2 – маса розчинника і розчиненої речовини відповідно, М2 – молярна маса розчиненої речовини;
Молярна частка (N2) – це відношення кількості молів розчиненої речовини (n2) до загальної кількості молів у системі, тобто до суми молів розчинника (n1) і всіх розчинених у ньому речовин. Для бінарного розчину:
(7.2); або (7.3)
Масова частка (W) – це відношення маси розчиненої речовини до маси розчину:
або (7.4)
де m1 – маса розчинника, г; m2 – маса розчиненої речовини, г;
Молярна концентрація еквіваленту (СН) – це кількість молів еквівалентів розчиненої речовини в 1 л розчину, (мольeкв)/л:
(7.5)
де me – еквівалентна маса, г/(мольекв); m – маса розчиненої речовини (г) в 1 л розчину; V – об’єм розчину в літрах.
Титр розчину (Т) – це маса розчиненої речовини, яка міститься у 1 мл розчину.
Приклади розв’язування типових задач
Приклад 1 У 450 г води розчинили 50 г CuSO4 5H2O. Обчислити масову частку кристалогідрату та безводної солі у розчині.
Розв’язування: Масова частка W = mречовини/mрозчину
W1 = mкристалогідр./mрозчину; W2 = /
mрозчину = 450+50 = 500 г; W1=50/500=0,1
W2 = де W3 =
Звідки W2 = або у відсотках: W1 = 0,1 100% = 10%;
W2 = 0,064100%=6,4%.
Приклад 2 Обчислити: а) відсоткову, б) СМ, СН, Сm концентрації розчину H3PO4, одержаного при розчиненні 18 г кислоти у 282 мл води, якщо густина розчину 1,031 г/см3.
Розв’язування: W=; CM = ν/V , моль/л;
СН = νекв/V, моль/л; m(р-ну) = 18+282=300 г
V(р-ну) = 300/1,031=291 мл або 0,291 л
Тоді W = ;
Звідки:
СМ = 0,184/0,290=0,63; СН = 0,552/0,291=1,90;
Приклад 3 Скільки грамів 32%-ного розчину нітратної кислоти необхідно додати до 600 г 80%-ного розчину тієї самої кислоти, щоб одержати 64%-ний розчин?
Розв’язування: Для розв’язання такого типу задач можна застосувати метод змішування (“правило хреста”). Записують концентрації вихідних розчинів і розчину, який потрібно одержати, як це показано на схемі:
80 32 ч (80%)
64
16 ч (32%)
48 ч (64%)
Як видно із наведеної схеми, на 32 частини 80%-ного розчину, необхідно взяти 16 ч 32%-ного розчину, тоді:
32 ч – 16 ч
600 ч – х г (32%-ного р-ну)
Маса нового розчину складає: m = 600 + 300 = 900 ч
Перевірка: в 900 ч 64%-ного розчину складає:
m = 900 0,64 = 576 г
Маса HNO3 в 600 г 80%-ного і 300 г 32%-ного розчинів дорівнює:
m = (600 0,8) + (300 0,32) = 480 + 96 = 576 г
Приклад 4 На нейтралізацію 20 мл розчину кислоти витрачено 10 мл розчину лугу (СН = 0,5). Чому дорівнює СН кислоти?
Розв’язування: Речовини взаємодіють між собою в однакових кількостях еквівалентів:
СН(лугу) V(лугу) = СН(к-та) V(к-та)
яснение:
Найдите наибольший корень уравнения
4log₆(3 -3/(2x+3) ) = 5log₆(2 +1/(x+1) ) + 4
ответ: - 2
Пошаговое объяснение: 4log₆(3 -3/(2x+3) ) =5log₆(2 +13/(x+1) ) + 4 ⇔
4log₆( 6(x+1)/(2x+3) ) = 5log₆( (2x+3)/(x+1) ) + 4 ⇔
4+4log₆(x+1)/(2x+3) = 5log₆(2x+3)/(x+1) ) + 4 ⇔
4log₆(x+1)/(2x+3) = - 5log₆ (x+1)/ (2x+3)) ⇔ 9log₆(x+1)/(2x+3) =0 ⇔
log₆ (x+1)/(2x+3) =0 ⇔ (x+1)/(2x+3) = 1 ⇔x+1=2x+3 ⇒ x= - 2
(единственный колень)