Тогда N = m/M, где - число Авогадро, M - молекулярная масса азота. Раз 30% молекул диссоциировали на атомы, то понятно, что число молекул в сосуде изменилось. Теперь в сосуде находятся молекулы в количестве 0,7·N и атомы, число которых равно 0,6 ·N. Парциальное давление газа равно = 0,7kTN/V, где k - постоянная Больцмана, T - абсолютная температура, а давление атомов равно = 0,6kTN/V.
Полное давление на стенки сосуда определяется суммой этих давлений P = + = 1,3RTm/(MV)
X = V0*t - a(t^2)/2 (1) { х1 = V0*t1 – а(t1^2)/2{ x2 = V0*t2 – а(t2^2)/2 (2)Имеем 1 = 5V0 – 12,5а (3)2 = 20V0 – 200а (4) Для того чтобы убрать скорость V0, умножим уравнение (3) на 4. Получим 4 = 20V0 – 50а (5)Отсюда имеем а = 1/75 = 0,01333… м/с^2 (6)5V0 = 12,5а + 1 = 12,5/75 + 1 = 0,166 + 1 =1,166. Тогда V0 = 1,166/5 = 0,2333 м/с. V1 = V0 – at = 0,2333 – (1/75)*1 = 0,2333 – 0,0133 = 0,22 м/с. - скорость шарика в конце первого отрезка пути (то есть при х = 1 м).ответ. Скорость шарика в конце первого отрезка пути (то есть когда шарик расстояние 1 м) V1 = 0,22 м/с.
N - число молекул в сосуде до начала диссоциации.
Тогда N =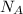 m/M, где
m/M, где 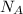 - число Авогадро, M - молекулярная масса азота.
- число Авогадро, M - молекулярная масса азота. 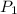 = 0,7kTN/V, где k - постоянная Больцмана, T - абсолютная температура, а давление атомов равно
= 0,7kTN/V, где k - постоянная Больцмана, T - абсолютная температура, а давление атомов равно 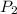 = 0,6kTN/V.
= 0,6kTN/V.
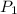 +
+ 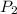 = 1,3RTm/(MV)
= 1,3RTm/(MV)
Раз 30% молекул диссоциировали на атомы, то понятно, что число молекул в сосуде изменилось. Теперь в сосуде находятся молекулы в количестве 0,7·N и атомы, число которых равно 0,6 ·N. Парциальное давление газа равно
Полное давление на стенки сосуда определяется суммой этих давлений
P =
Подставляем данные, и вуаля!
ответ: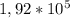 Па
Па