1850 Дж / (кг*К)
Объяснение:
1)
Для гелия:
ν₁ = m₁ / M₁
Отсюда
m₁ = ν₁*M₁ = 2*4*10⁻³ = 8*10⁻³ кг
Для кислорода:
ν₂ = m₂ / M₂
Отсюда
m₂ = ν₂*M₂ = 3*16*10⁻³ = 48*10⁻³ кг
Суммарная масса смеси:
m = m₁ + m₂ = (8+48)*10⁻³ = 56*10⁻³ кг
2)
Находим массовые доли газов:
ω₁ = m₁ / m = 8*10⁻³ / 56*10⁻³ ≈ 0,14
ω₂ = m₂ / m = 48*10⁻³ / 56*10⁻³ ≈ 0,86
3)
Удельная теплоемкость гелия (число степеней свободы двухатомного газа i = 3)
cp₁ = ((i+2)/2)*R/M = ((3+2)/2)*8,31 / 4*10⁻³ ≈ 5 200 Дж / (кг*К)
Для кислорода:
cp₂ = ((i+2)/2)*R/M = ((3+2)/2)*8,31 / 16*10⁻³ ≈ 1 300 Дж / (кг*К)
4)
Для смеси:
cp = cp₁*ω₁ + cp₂*ω₂ = 5200*0,14 + 1300*0,86 ≈ 1 850 Дж/(кг*К)
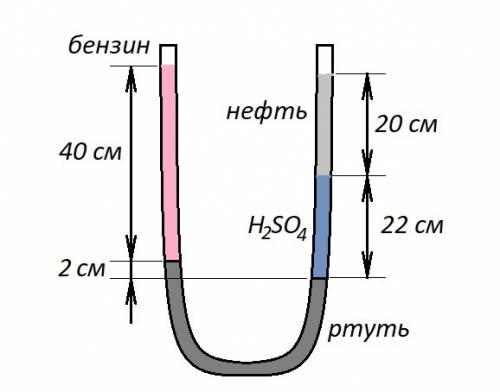
1-ртуть
2-бензин
3-серная кислота
4-нефть
давление в левом колене равно давлению в правом колене
Pл =Pпр
P1+P2 = P3+P4
ρ- плотность жидкости
g-ускорение св.падения
h-высота столба жидкости
ρ1 g h1 + ρ2 g h2 = ρ3 g h3 + ρ4 g h4
ρ1 h1 + ρ2 h2 = ρ3 h3 + ρ4 h4
ρ3 h3 = ρ1 h1 + ρ2 h2 - ρ4 h4
ρ3 = (ρ1 h1 + ρ2 h2 - ρ4 h4) /h3
ρ1 = 13,6 г/см3; h1 = 2 см
ρ2 = 0,7 г/см3; h2 = 40 см
ρ3 = ? ; h3 = 22 см
ρ4 = 0,8 г/см3; h4 = 20 см
ρ3 = (13,6 * 2 + 0,7 * 40 - 0,8 * 20) / 22 = 1,8 г/см3;
ответ
ρ3 = 1,8 г/см3;
ответ: у всех колебаний период один и тот же и равен 8 с.
Объяснение: