α=60°
m1=m2=m=1кг
μ=0,3
a1=a2=a-?
T-?
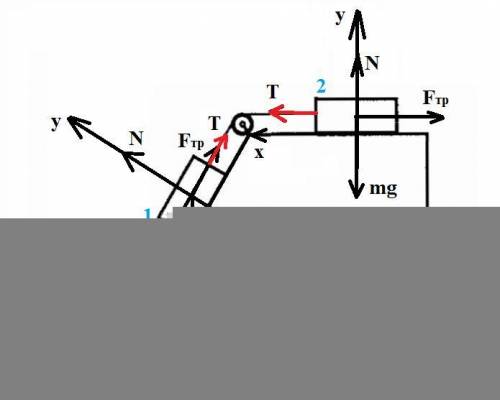
Рисунок с силами в прикрепленном файле
Дано:
ma=∑F
1 тело:
ОУ: 0=N-mg*cosα ⇒ N=mg*cosα
ОХ: ma=mg*sinα-Fтр-T; ma=mg*sinα-μN-T; ma=mg*sinα-μmg*cosα-T
2 тело:
ОУ: 0=N-mg ⇒ N=mg
ОХ: ma=T-Fтр; ma=T-μN; ma=T-μmg
Чтобы найти а, сложим получившиеся равенства.
ma=mg*sinα-μmg*cosα-T
+
ma=T-μmg
=
2ma=mg*sinα-μmg*cosα-μmg
а=mg(sinα-μ*cosα-μ)/2m
а=g(sinα-μ*cosα-μ)/2=9,8(√3/2-0,5*0,3-0,3)/2=2 м/с²
ma у первого и второго тела равны. Приравняем их и выведем Т.
T-μmg=mg*sinα-μmg*cosα-T
2Т=mg*sinα-μmg*cosα+μmg
Т=mg(sinα-μ*cosα+μ)/2=1*9,8(√3/2-0,3*0,5+0,3)/2≈5Н
a=2 м/с²
Т=5Н
Електроліз полягає в електрохімічних процесах окиснення та відновлення на електродах. При електролізі позитивно заряджені йони рухаються до катода, на якому електрохімічно відновлюються. Негативно заряджені йони рухаються до анода, де електрохімічно окиснюються.
Хімічні зміни, спричинювані пропусканням електричного струму через розплавлену йонну сполуку або через розчин, який містить йони. Їх зумовлює сукупнiсть хімiчних реакцiй, що протiкають пiд дiєю електричного струму на електродах, занурених в електролiт, при цьому на катодi вiдбувається вiдновлення, а на анодi окиснення йонiв електролiту.
В результаті електролізу на електродах виділяються речовини в кількостях, пропорційних кількості пропущеного струму. Електроліз застосовується для одержання багатьох речовин
ответ: 25 В.