Физические свойства. Бутадиен-1,3 — легко сжижающийся газ с неприятным запахом. Изопрен — жидкость с tкип 34 °С.
Получение. Основной промышленный получения диенов — дегидрирование алканов. Бутадиен-1,3 (дивинил) получают из бутана:
t,Сr2О3 СН3-СН2-СН2-СН3 → СН2=СН-СН=СН2 + 2Н2,
а изопрен (2-метилбутадиен-1,3) — из 2-метилбутана:
t, Сr2О3 СН3-СН(СН3)-СН2-СН3 → СН2=С(СН3)-СН=СН2+2Н2.
Бутадиен-1,3 можно также получать по реакции Лебедева путем одновременного дегидрирования и дегидратации этанола:
t, ZnO, Al2O3 2С2Н5ОН → СН2=СН-СН=СН2 + Н2 + 2Н2О.
Химические свойства. Для алкадиенов характерны обычные реакции электрофильного присоединения АE, свойственные алкенам. Особенность сопряженных диенов состоит в том, что две двойные связи в их молекулах функционируют как единое целое, поэтому реакции присоединения могут протекать в двух направлениях: а) к одной из двойных связей (1,2-присоединение) или б) в крайние положения сопряженной системы с образованием новой двойной связи в центре системы (1,4-присоединение). Так, присоединение брома к бутадиену может привести к двум продуктам:
1,2 СН2=СН-СН=СН2 + Вr2 → СН2=СН-СНВr-СН2Вrили
1,4 СН2=СН-СН=СН2 + Вr2 → ВrСН2-СН=СН-СН2ВrПодбор реагентов и условий реакций позволяет направлять присоединение по любому из двух направлений.
Важнейшее свойство диенов — их к полимеризации, которая используется для получения синтетических каучуков. При полимеризации бутадиена-1,3, которая протекает как 1,4-присоединение, получают бутадиеновый каучук:
nСН2=СН-СН=СН2 → (-СН2-СН=СН-СН2-)n.
Использование металлоорганических катализаторов в этой реакции позволяет получить каучук с регулярным строением, в котором все звенья цепи имеют цис-конфигурацию. Аналогичная реакция с изопреном дает синтетический изопреновый каучук, который по строению и свойствам близок к природному каучуку:
nСН2=С(СН3)-СН=СН2 → (-СН2-С(СН3)=СН-СН2-)n.
Применение. Основная область применения алкадиенов - синтез каучуков.
Основное уравнение молекулярно-кинетической теории газов:
з=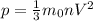 (v - средний квадрат скорости молекул)
(v - средний квадрат скорости молекул)
Концентрация молекул газа - это по сути и есть плотность газа, а она равна:
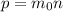 (p - плотность газа)
(p - плотность газа)
Подставим это выражение в основное уравнение молекулярно-кинетической теории газов:
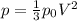 (Pо - плотность или концентрация молекул в газе)
(Pо - плотность или концентрация молекул в газе)
Концентрация увеличилась, а квадрат скорости уменьшился в заданное количество раз. Подставляем эти коэффициенты:
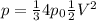
При упрощении этого выражения мы увидим, что давление увеличилось в два раза.
ответ: 2 раза.
Рт= Рж/4, Рт-плотн. тела, Рж - плотн. жидк. FA = Рж х 9.8 х Vп, где Vп -объм погруженной части тела. Учитывая все записать Рж х9.8 х Vп =Рж /4 х 9.8 х V, V - объм тела. Отсюда Vп = V /4, V - Vп -объм погруженной части тела. Объем погруженной части / весь объем = 4-1 /4 =3/4 Такая часть выступает над поверхностью Этот результат умножить на 0.0002 и перевести в см3, 1м3= 10(в шестой) см3. Отв. 150см3