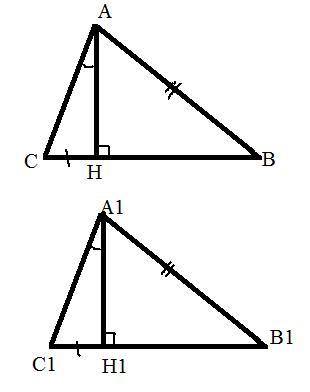
Объяснение:
Дано: AB = A1B1, CH=C1H1, <CAH=<C1A1Н1. АН, А1Н1 - высоты.
Доказать: △АВС=△А1В1С1.
Док-во:
Рассмотрим △АСН и △А1С1Н1. Они прямоугольные и у них CH=C1H1 - катеты, <CAH=<C1A1Н1 - острые углы. Значит △АСН=△А1С1Н1 по 4 признаку (по катету и острому углу). => АС=А1С1, АН=А1Н1.
Рассмотрим △АВН и △А1В1Н1. Они прямоугольные и у них АН=А1Н1 - катеты, AB = A1B1 - гипотенузы. Значит △АВН=△А1В1Н1 по 2 признаку (по катету и гипотенузе). => ВН=В1Н1.
CH=C1H1, ВН=В1Н1, CB=CH+HB, C1B1=C1H1+H1B1 => CB=C1B1.
Таким образом для треугольников △АВС и △А1В1С1 имеем, что AB = A1B1, АС=А1С1, CB=C1B1, значит △АВС=△А1В1С1 по 3му признаку (по 3м сторонам), чтд.
2. Взаимодействие кислот с металлами.
Кислоты взаимодействуют с металлами, стоящими в ряду активности металлов левее водорода. В результате реакции образуется соль и выделяется водород Mg+2HCl→MgCl2+H2↑
3. Взаимодействие кислот с основными и амфотерными оксидами.
Кислоты реагируют с основными и амфотерными оксидами. В результате реакции обмена образуются соль и вода.
K2O+2HNO3→2KNO3+H2O,
Al2O3+6HCl→2AlCl3+3H2O.
4. Взаимодействие кислот с основаниями и с амфотерными гидроксидами.
Кислоты реагируют с основаниями и с амфотерными гидроксидами, образуя соль и воду.
KOH+HNO3→KNO3+H2O,
Al(OH)3+3HCl→AlCl3+3H2O.
5. Взаимодействие кислот с солями.
Реакции обмена между кислотами и солями возможны, если в результате образуется практически нерастворимое в воде вещество (выпадает осадок), образуется летучее вещество (газ) или слабый электролит.
А) Кислоты реагируют с растворами солей, если в результате реакции один из продуктов выпадает в осадок.
H2SO4+BaCl2→BaSO4↓+2HCl,
Na2SiO3+2HNO3→H2SiO3↓+2NaNO3.
Б) Продукт реакции при обычных условиях, либо при нагревании, улетучивается.
NaCl(тв.)+H2SO4(конц.)→Na2SO4+2HCl↑,
FeS+2HCl→FeCl2+H2S↑.
В) Если кислота, которая вступает в реакцию, является сильным электролитом, то кислота, которая образуется — слабым.
6. Разложение кислородсодержащих кислот.
При разложении кислот образуются кислотный оксид и вода. Угольная кислота разлагается при обычных условиях, а сернистая и кремниевая кислота — при небольшом нагревании:
H2CO3⇄H2O+CO2↑,
H2SO3⥫⥬toH2O+SO2↑,H2SiO3−→−toSiO2+H2O.
Если кратко и без примеров:
изменяют цвет индикаторов,
реагируют с металлами,
реагируют с основными и амфотерными оксидами,
реагируют с основаниями и амфотерными гидроксидами,
реагируют с солями,
некоторые кислоты легко разлагаются.