Задание 1:
1) Сложные вещества, состоящие из двух элементов, один из которых кислород - ОКСИДЫ
2) Сложные вещества, состоящие из разных по виду атомов химических элементов - СЛОЖНЫЕ ВЕЩЕСТВА
3) Вещества, состоящие из ионов металла и гидроксильных групп - ОСНОВАНИЯ
4) Вещества, состоящие из ионов металла и кислотных остатков - СОЛИ
5) Вещества-распознаватели кислот и щелочей - ИНДИКАТОРЫ
Задание 2:
1) в глаз попала кислота - промыть глаза большим количеством воды около 30 минут
2) если на кожу попала кислота - промыть большим количеством воды, после промыть раствором пищевой соды
3) ожог щелочами - промыть водой, после раствором лимонной, уксусной или борной кислоты
Задание 3:
А - 4
Б - 5
В - 1
Г - 2
Д - 3
Задание 4:
А. Лишнее Cu(OH)₂, потому что из всех перечисленных оснований оно единственное не растворимо в воде
Б. Лишнее LiOH, потому что из всех перечисленных оснований в этом основании единственный металл имеет степень окисления +1, когда все остальные +2
В. Лишнее Al(OH)₃, потому что из всех перечисленных оснований, во-первых, это нерастворимое, во-вторых, металл в нем имеет степень окисления +3, когда все остальные +1
Задание 5:
а) оксиды: CO₂ (оксид углерода (IV)), Al₂O₃ (оксид алюминия), Na₂O (оксид натрия)
б) основания: NaOH (гидроксид натрия или едкий натр), Fe(OH)₃ (гидроксид железа (III)), Ba(OH)₂ (гидроксид бария)
в) кислоты: HNO₃ (азотная кислота), H₂CO₃ (угольная кислота)
г) соли: K₂SO₄ (сульфат калия), Mg₃(PO₄)₂ (фосфат магния), CuCl₂ (хлорид меди)
Задание 6:
Формула: 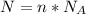 , где
, где 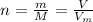 - количество вещества (моль);
- количество вещества (моль); 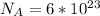 - число Авогадро (1/моль).
- число Авогадро (1/моль).
M - молярная масса (считается как сумма атомных масс элементов, входящих в вещество; атомные массы даны в таблице Менделеева)
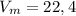 - молярный объем, одинаковый для всех газов при н.у. (л/моль)
- молярный объем, одинаковый для всех газов при н.у. (л/моль)
Считаем:
а) 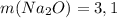 г
г
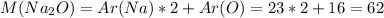 г/моль
г/моль
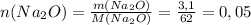 моль
моль
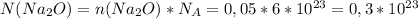 молекул
молекул
б) 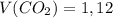 л
л
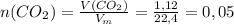 моль
моль
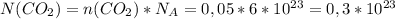 молекул
молекул
Характеристика натрия:
1) Название элемента -натрий, химический символ - Na, порядковый номер - № 11 ,
атомная масса Ar=23 Группа - 1, подгруппа- главная , 3-й период
Заряд ядра атома натри я Z=+11 (в ядре 11 протонов- p⁺ и 12 нейтронов - n⁰)
Вокруг ядра атома 3 энергетических уровня, на которых располагаются 11 электрона.
3) Исходя из вышеизложенного, напишем строение атома натрия и его электронную формулу:
а). Модель атома натрия при дуг: ₊₁₁Na)₂)₈)₁
б). Модель атома- электронная формула (электронная конфигурация):
а) электронная формула натрия ₊₁₁Na 1s²2s²2p⁶3s¹
в).Электронно-графическая модель атома натрия:
3уровень s ↑
p ⇅ ⇅ ⇅
2уровень s ⇅
1уровень s ⇅
₊₁₁Na
4. Простое вещество натрий щелочной металл, состоит из одного атома , валентность натрия в соединениях равна 1, степень окисления+1 . Натрий –восстановитель.
5. Молекулы атомов в 1 группе, главной подгруппе одноатомные. С увеличением заряда ядра от лития до франция неметаллические свойства уменьшаются, а металлические усиливаются.
6. Молекулы атомов простых веществ в периоде: натрий, магний, алюминий, кремний -
одноатомные; фосфора четырехтомные P₄, серы многоатомные (S)n,хлора двухатомные CI₂. От натрия к хлору меняются свойства веществ: натрий, магний - металлы, алюминий -амфотерный металл, кремний полуметалл, фосфор, сера, хлор - неметаллы. Также слева направо в периоде меняются окислительно-восстановительные свойства. Натрий, магний, алюминий - восстановители. Кремний, фосфор, сера, хлор - могут быть как восстановителями, так окислителями.
7. Формула высшего оксида: Na2O – основной оксид
8. Формула гидроксида: NaOH- основание растворимое в воде, щелочь
9. Летучего соединения с водородом не образует, а соединение натрия с водородом - это гидрид натрия NaH₂ -представляет собой при стандартных условиях бесцветные кубические ионной кристаллической решёткой.. Является сильным восстановителем. Воспламеняется в атмосфере некоторых галогенов: фтора, хлора, а также при 230 °C в кислороде. При нагревании до 300 °C в вакууме гидрид натрия разлагается.
Характеристика хлора:
1. Элемент №17 хлор, его атомная масса Ar=35,5 (два изотопа Ar =35. Ar = 37 ), его заряд ядра Z=+17, в ядре 17 p⁺(протонов) 18 n⁰ (нейтронов). Вокруг ядра находятся 17 e⁻(электронов), которые размещаются на трех энергетических уровнях, так как хлор находится в третьем периоде.
1). Модель атома хлора при дуг: ₊₁₇CI)₂)₈)₇
2). Модель атома, через электронную формулу (электронная
конфигурация): ₊₁₇CI 1s²2s²2p⁶3s²3p⁵
3). Электронно-графическая модель атома:
p ⇵ ⇵ ↑
3уровень s ⇵
p ⇅ ⇅ ⇅
2уровень a ⇅
1уровень s ⇅
₊₁₇CI
2. Молекула простого вещества хлора двухатомная. Молекулы атомов простых веществ в периоде: натрий, магний, алюминий, кремний - одноатомные; фосфора четырехтомные P₄, серы многоатомные (S)n, хлора двухатомные CI₂. От натрия к хлору меняются свойства веществ: натрий, магний - металлы, алюминий -амфотерный металл, кремний полуметалл, фосфор, сера, хлор - неметаллы. Также слева направо в периоде меняются окислительно-восстановительные свойства. Натрий, магний, алюминий -восстановители. Кремний, фосфор, сера, хлор - могут быть как восстановителями, так окислителями.
3. Молекулы атомов в 7 группе, главной подгруппе хлора двухатомные. С увеличением заряда ядра от фтора до астата неметаллические свойства уменьшаются, а металлические усиливаются.
4. Высший оксид хлора–CI₂O₇, кислотный оксид:
5. Гидроксид – HCIO₄ , хлорная , сильная кислота,
6. Летучее соединение с водородом HCI хлороводород, бесцветный
газ, с неприятным запахом, хорошо растворим в воде, раствор соляная кислота HCI.